Aktīvās sastāvdaļas: Fingolimods
GILENYA 0,5 mg cietās kapsulas
Indikācijas Kāpēc lieto Gilenya? Kam tas paredzēts?
Kas ir Gilenya
Gilenya aktīvā sastāvdaļa ir fingolimods.
Kam domāta Gilenya
Gilenya lieto pieaugušajiem recidivējoši remitējošas multiplās sklerozes (MS) ārstēšanai, īpaši:
Pacienti, kuri nav reaģējuši uz terapiju ar MS ārstēšanu.
vai
Pacienti ar strauji progresējošu smagu MS.
Gilenya neārstē MS, bet palīdz samazināt recidīvu skaitu un palēnina MS izraisītās fiziskās invaliditātes progresēšanu.
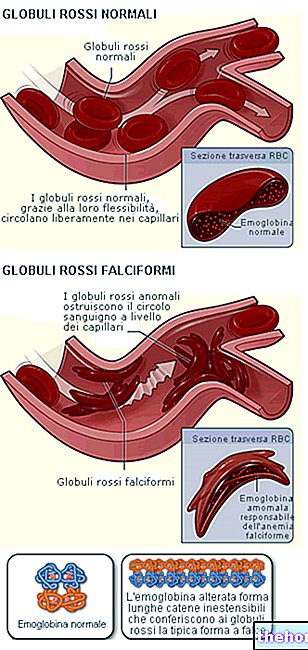
Kas ir multiplā skleroze
MS ir hroniska slimība, kas ietekmē centrālo nervu sistēmu (CNS), kas ietver smadzenes un muguras smadzenes. MS gadījumā iekaisums iznīcina aizsargapvalku (ko sauc par mielīnu), kas izklāta nervus CNS un neļauj nerviem darboties kā vajadzētu.Šo procesu sauc par demielinizāciju.
Recidivējoši remitējošu MS raksturo neiroloģisku simptomu recidīvi (recidīvi), kas atspoguļo centrālās nervu sistēmas iekaisuma stāvokli. Simptomi dažādiem pacientiem ir atšķirīgi, bet parasti tie ietver grūtības staigāt, nejutīgumu, redzes vai līdzsvara traucējumus. Recidīva simptomi var pilnībā izzust, kad recidīvs ir beidzies, bet dažas sūdzības var saglabāties.
Kā darbojas Gilenya
Gilenya palīdz aizsargāt nervu sistēmu no imūnsistēmas uzbrukumiem, samazinot dažu balto asins šūnu (limfocītu) spēju brīvi cirkulēt organismā un neļaujot tām nokļūt smadzenēs un muguras smadzenēs. Tas ierobežo MS izraisītos nervu bojājumus.
Kontrindikācijas Kad Gilenya nedrīkst lietot
Nelietojiet Gilenya
- ja Jums ir samazināta imūnreakcija (imūndeficīta sindroma, slimības vai imūnsistēmu nomācošu zāļu dēļ).
- ja Jums ir smaga infekcija vai hroniska infekcija, piemēram, hepatīts vai tuberkuloze.
- ja Jums ir aktīvs vēzis (izņemot, ja tas ir ādas vēža veids, ko sauc par bazālo šūnu ādas vēzi).
- ja Jums ir smagi aknu darbības traucējumi.
- ja Jums ir alerģija pret fingolimodu vai kādu citu šo zāļu sastāvdaļu.
Ja kaut kas no iepriekš minētā attiecas uz Jums, pastāstiet savam ārstam pirms Gilenya lietošanas.
Piesardzība lietošanā Kas jāzina pirms Gilenya lietošanas
Pirms Gilenya lietošanas konsultējieties ar ārstu:
- ja Jums ir neregulāra, patoloģiska sirdsdarbība.
- ja Jums rodas zemas sirdsdarbības simptomi (piemēram, reibonis, slikta dūša vai sirdsklauves).
- ja Jums ir kādi sirdsdarbības traucējumi, sirds asinsvadu aizsprostojums, agrāk ir bijis sirdslēkme vai sirdsdarbības apstāšanās vai Jums ir stenokardija.
- ja Jums agrāk ir bijis insults.
- ja Jums ir sirds mazspēja.
- ja miega laikā Jums ir smagas elpošanas problēmas (smaga miega apnoja).
- ja Jums ir teikts, ka Jums ir patoloģiska EKG.
- ja Jūs lietojat vai nesen esat lietojis zāles pret neregulāru sirdsdarbību, piemēram, hinidīnu, disopiramīdu, amiodaronu vai sotalolu.
- ja Jūs lietojat vai nesen esat lietojis zāles, kas palēnina sirdsdarbību (piemēram, beta blokatorus, verapamilu, diltiazēmu vai ivabradīnu, digoksīnu, antiholīnesterāzes zāles vai pilokarpīnu).
- ja Jums kādreiz ir bijušas pēkšņas samaņas zuduma vai ģībšanas epizodes (ģībonis).
- ja plānojat vakcinēties.
- ja Jums nekad nav bijušas vējbakas.
- ja Jums ir vai ir bijuši redzes traucējumi vai citas pietūkuma pazīmes acs aizmugures centrālajā redzes zonā (makulā) (stāvoklis, kas pazīstams kā makulas tūska, skatīt zemāk), ja Jums ir vai ir bijis "iekaisums vai" acs infekcija (uveīts) vai ja Jums ir diabēts (kas var izraisīt acu problēmas).
- ja Jums ir aknu darbības traucējumi.
- ja Jums ir augsts asinsspiediens, ko nevar kontrolēt ar zālēm.
- ja Jums ir smagi plaušu darbības traucējumi vai smēķēšanas izraisīts klepus.
Ja kaut kas no iepriekš minētā attiecas uz Jums, pastāstiet savam ārstam pirms Gilenya lietošanas.
Lēna sirdsdarbība (bradikardija) un neregulāra sirdsdarbība: Ārstēšanas sākumā Gilenya izraisa sirdsdarbības palēnināšanos. Tā rezultātā var rasties reibonis vai nogurums, sirdsdarbības apziņa vai asinsspiediena pazemināšanās. ārsts, jo Jums var būt nepieciešama tūlītēja ārstēšana. Gilenya var izraisīt arī neregulāru sirdsdarbību, īpaši pēc pirmās devas. Neregulāra sirdsdarbība parasti normalizējas mazāk nekā dienā. Lēna sirdsdarbība parasti atgriežas normālā stāvoklī mēneša laikā.
Ārsts lūgs jums palikt klīnikā vai slimnīcā vismaz 6 stundas pēc pirmās Gilenya devas ievadīšanas, kuras laikā pulss un asinsspiediens tiks mērīts jebkurā laikā: tādā veidā var veikt atbilstošus pasākumus blakusparādības, kas rodas ārstēšanas sākumā. Jums ir jābūt pieejamai elektrokardiogrammai pirms pirmās Gilenya devas un 6 stundu uzraudzības beigās. Jūsu ārsts var nepārtraukti pārbaudīt jūsu elektrokardiogrammu šajā periodā. Ja pēc 6:00 stundas Jūsu sirdsdarbības ātrums ir ļoti zems vai samazinās, vai ja EKG parāda novirzes, iespējams, ka jums būs nepieciešams novērot ilgāku laiku (vismaz vēl 2 stundas un, iespējams, līdz nākamajam rītam), līdz šīs problēmas tiks atrisinātas. tas pats var notikt, ja viņa atkal uzņems G ilenya pēc ārstēšanas pārtraukšanas, atkarībā no tā, cik ilgs bija pārtraukums un cik ilgi esat lietojis Gilenya pirms pārtraukuma.
Ja Jums ir vai pastāv neregulāras vai patoloģiskas sirdsdarbības risks, ja EKG ir patoloģiska vai ja Jums ir sirds slimība vai sirds mazspēja, Gilenya var nebūt jums piemērots.
Ja Jums kādreiz ir bijušas pēkšņas samaņas zuduma epizodes vai samazināts sirdsdarbības ātrums, Gilenya var nebūt Jums piemērots. Pie jums ieradīsies kardiologs (sirds speciālists), kurš ieteiks, kā sākt ārstēšanu ar Gilenya, ieskaitot uzraudzību līdz nākamajam rītam.
Ja lietojat zāles, kas var izraisīt sirdsdarbības ātruma samazināšanos, Gilenya var nebūt jums piemērots. Jūs apmeklēs kardiologs, kurš novērtēs, vai varat kā alternatīvu lietot zāles, kas nesamazina sirdsdarbību, un ļaus Jums sākt ārstēšanu ar Gilenya. Ja šīs terapijas izmaiņas nav iespējamas, kardiologs jums ieteiks, kā sākt ārstēšanu ar Gilenya, ieskaitot uzraudzību līdz nākamajam rītam.
Ja jums nekad nav bijušas vējbakas: Ja jums nekad nav bijis vējbakas, ārsts pārbaudīs jūsu imunitāti pret vīrusu, kas to izraisa (varicella zoster vīruss). Ja neesat aizsargāts pret vīrusu, pirms ārstēšanas uzsākšanas ar Gilenya jums var būt nepieciešama vakcinācija. Ja tā notiek, ārsts atliks Gilenya terapijas uzsākšanu līdz vienam mēnesim pēc pilna vakcinācijas kursa pabeigšanas.
Infekcijas: Gilenya samazina balto asins šūnu (īpaši limfocītu) skaitu. Baltās asins šūnas cīnās ar infekcijām. Gilenya lietošanas laikā (un līdz 2 mēnešiem pēc ārstēšanas pārtraukšanas) jūs varat vieglāk inficēties. Jebkura esošā infekcija var pasliktināties. Infekcijas var būt nopietnas un dzīvībai bīstamas. Ja domājat, ka Jums ir infekcija, ja Jums ir drudzis, ja Jums ir gripas simptomi vai ja Jums ir galvassāpes, ko pavada stīvs kakls, jutība pret gaismu, slikta dūša un / vai apjukums (tie var būt meningīta simptomi), sazinieties ar savu uzreiz ārsts ..
Makulas tūska: pirms ārstēšanas uzsākšanas ar Gilenya, ja Jums ir vai ir bijuši redzes traucējumi vai citas pietūkuma pazīmes acs aizmugurē esošajā centrālajā redzes zonā (makulā), ja Jums ir vai ir bijusi acs iekaisums vai infekcija (uveīts) vai ja Jums ir diabēts, ārsts var lūgt veikt acu pārbaudi.
Ārsts var lūgt jums veikt acu pārbaudi 3-4 mēnešus pēc ārstēšanas uzsākšanas ar Gilenya.
Makula ir neliela tīklenes zona, kas atrodas acs aizmugurē, kas ļauj skaidri un asi redzēt formas, krāsas un detaļas. Gilenya var izraisīt makulas pietūkumu - stāvokli, kas pazīstams kā makulas tūska. pietūkums, parasti pirmajos 4 ārstēšanas mēnešos ar Gilenya.
Makulas tūska, visticamāk, rodas, ja Jums ir diabēts vai ir bijis “acs iekaisums”, ko sauc par uveītu. Šādos gadījumos ārsts vēlēsies regulāri pārbaudīt, vai nav pirmās makulas tūskas pazīmes.
Ja Jums ir bijusi makulas tūska, pirms ārstēšanas ar Gilenya atsākšanas konsultējieties ar ārstu.
Makulas tūska var izraisīt dažus vizuālos simptomus (optisko neirītu), kas rodas arī MS uzbrukumu laikā. Sākotnējā stadijā simptomi var nebūt. Noteikti pastāstiet ārstam par jebkādām redzes izmaiņām. Ārsts var lūgt atsaukties uz tām iziet acu pārbaudi, īpaši, ja:
- centrālā skata zona nav fokusēta vai tajā ir ēnas;
- centrālās redzes zonā veidojas akla vieta;
- ir grūtības atšķirt krāsas vai smalkas detaļas.
Aknu darbības testi: ja Jums ir smagi aknu darbības traucējumi, nevajadzētu lietot Gilenya. Ārstēšana ar Gilenya var ietekmēt jūsu aknu darbību. Jūs, visticamāk, nepamanīsit nekādus simptomus, bet, ja pamanāt ādas vai acu baltumu dzeltēšanu, neparastu tumšu urīnu vai neizskaidrojamu sliktu dūšu un vemšanu, nekavējoties informējiet par to ārstu.
Ja pēc Gilenya terapijas uzsākšanas Jums rodas kāds no šiem simptomiem, lūdzu, nekavējoties informējiet par to ārstu.
Pirmajos divpadsmit ārstēšanas mēnešos ārsts lūgs Jums veikt asins analīzes, lai pārbaudītu aknu darbību. Ja rezultāti liecina, ka ir aknu darbības traucējumi, ārstēšana ar Gilenya var būt jāpārtrauc.
Augstspiediena
Tā kā Gilenya izraisa nelielu asinsspiediena paaugstināšanos, ārsts var regulāri pārbaudīt asinsspiedienu. Plaušu problēmas Gilenya vāji ietekmē plaušu darbību. Pacientiem ar smagām plaušu problēmām vai smēķēšanas izraisītu klepu blakusparādības var rasties vieglāk.
Asins skaitļi Gilenya terapijas vēlamais efekts ir samazināt balto asins šūnu daudzumu asinīs. Tās parasti normalizējas 2 mēnešu laikā pēc ārstēšanas pārtraukšanas. Ja Jums ir jāveic asins analīzes, lūdzu, pastāstiet ārstam, ka lietojat Gilenya. .
Pirms ārstēšanas uzsākšanas ar Gilenya ārsts apstiprinās, vai jūsu balto asins šūnu skaits ir pietiekams, un var lūgt regulāri atkārtot skaitīšanu. Ja jums nav pietiekami daudz balto asins šūnu, jums, iespējams, būs jāpārtrauc Gilenya lietošana.
Aizmugurējās atgriezeniskās encefalopātijas sindroms (PRES)
Pacientiem ar multiplo sklerozi, kas ārstēti ar Gilenya, reti ziņots par sindromu, ko sauc par aizmugurējo atgriezenisko encefalopātiju (PRES). Simptomi var būt pēkšņas stipras galvassāpes, apjukums, krampji un redzes izmaiņas. Pastāstiet ārstam, ja ārstēšanas laikā ar Gilenya rodas kāds no šiem simptomiem.
Lietošana gados vecākiem cilvēkiem
Pieredze ar Gilenya lietošanu gados vecākiem pacientiem, kas vecāki par 65 gadiem, ir ierobežota. Ja jums ir kādi jautājumi, vaicājiet ārstam.
Bērni un pusaudži
Gilenya nav paredzēts lietošanai bērniem un pusaudžiem līdz 18 gadu vecumam, jo tas nav pētīts MS pacientiem līdz 18 gadu vecumam.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Gilenya iedarbību
Pastāstiet ārstam vai farmaceitam par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot. Pastāstiet ārstam, ja lietojat kādu no šīm zālēm:
- Zāles, kas nomāc vai maina imūnsistēmu, ieskaitot citas zāles, ko lieto MS ārstēšanai, piemēram, beta interferonu, glatiramera acetātu, natalizumabu, mitoksantronu, teriflunomīdu, dimetilfumarātu vai alemtuzumabu. Jūs nedrīkstat lietot Gilenya kopā ar šīm zālēm, jo tās var pastiprināt ietekmi uz imūnsistēmu (skatīt arī "Nelietojiet Gilenya šādos gadījumos").
- Kortikosteroīdi, ņemot vērā iespējamo papildinošo ietekmi uz imūnsistēmu.
- Vakcīnas. Ja Jums nepieciešama vakcinācija, vispirms jautājiet padomu savam ārstam. Gilenya terapijas laikā un 2 mēnešus pēc tās Jūs nedrīkstat saņemt dažu veidu vakcīnas (novājinātas dzīvās vakcīnas), jo tās var izraisīt infekciju, kuru tām vajadzēja novērst. Citas vakcīnas var nedarboties tik labi kā parasti, ja tās tiek ievadītas šajā laikā ...
- Zāles, kas palēnina sirdsdarbību (piemēram, beta blokatori, piemēram, atenolols). Gilenya vienlaicīga lietošana ar šīm zālēm var pastiprināt ietekmi uz sirdsdarbību pirmajās Gilenya terapijas dienās.
- Zāles neregulāras sirdsdarbības ārstēšanai, piemēram, hinidīns, disopiramīds, amiodarons vai sotalols. Ārsts var izlemt neizrakstīt Gilenya, ja lietojat šāda veida zāles, jo tās var pastiprināt ietekmi uz neregulāru sirdsdarbību.
- Citas zāles:
- proteāzes inhibitori, pretinfekcijas līdzekļi, piemēram, ketokonazols, azola pretsēnīšu līdzekļi, klaritromicīns vai telitromicīns.
- karbamazepīns, rifampicīns, fenobarbitāls, fenitoīns, efavirenzs vai asinszāle (potenciāls efektivitātes samazināšanās risks).
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība un zīdīšanas periods
Pirms uzsākt ārstēšanu ar Gilenya, ārsts var lūgt jums veikt grūtniecības testu, lai pārliecinātos, ka neesat stāvoklī. Gilenya lietošanas laikā vai divus mēnešus pēc ārstēšanas pārtraukšanas jāizvairās no grūtniecības iestāšanās, jo pastāv risks kaitēt bērnam. Konsultējieties ar savu ārstu par drošām kontracepcijas metodēm, ko lietot ārstēšanas laikā. Ar Gilenya un 2 mēnešus pēc ārstēšanas pārtraukšanas .
Ja Gilenya lietošanas laikā Jums iestājas grūtniecība, pārtrauciet ārstēšanu un nekavējoties informējiet ārstu. Ārsts kopā ar jums izlems, kas ir labākais jums un jūsu mazulim.
Gilenya lietošanas laikā nebarojiet bērnu ar krūti. Gilenya izdalās mātes pienā, radot nopietnu blakusparādību risku jaundzimušajam.
Pirms jebkuru zāļu lietošanas konsultējieties ar ārstu vai farmaceitu.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Ārsts jums pateiks, vai jūsu slimība ļauj droši vadīt transportlīdzekli un apkalpot mehānismus. Nav sagaidāms, ka Gilenya ietekmēs spēju vadīt transportlīdzekļus un apkalpot mehānismus.
Tomēr ārstēšanas sākumā jums būs jāpaliek ārsta kabinetā vai slimnīcā 6 stundas pēc pirmās Gilenya devas lietošanas. Spēja vadīt transportlīdzekli un apkalpot mehānismus var tikt traucēta šajā laikā un, iespējams, arī pēc tam.
Devas un lietošanas veids Kā lietot Gilenya: Devas
Ārstēšanu ar Gilenya uzraudzīs ārsts, kuram ir pieredze multiplās sklerozes ārstēšanā.
Vienmēr lietojiet šīs zāles tieši tā, kā ārsts Jums stāstījis.
Ja rodas šaubas, konsultējieties ar ārstu. Deva ir viena kapsula vienu reizi dienā. Lietojiet Gilenya vienu reizi dienā, uzdzerot glāzi ūdens. Gilenya var lietot kopā ar ēdienu vai bez tā.
Gilenya lietošana katru dienu vienā un tajā pašā laikā palīdzēs atcerēties, kad zāles jālieto.
Nepārsniedziet ieteicamo devu.
Ārsts var pāriet tieši no ārstēšanas ar beta interferonu, glatiramera acetātu vai dimetilfumarātu uz Gilenya, ja nav iepriekšējās ārstēšanas izraisītu noviržu pazīmju. Jūsu ārsts var likt jums veikt asins analīzi, lai izslēgtu šīs novirzes. Pēc natalizumaba lietošanas pārtraukšanas var būt jāgaida 2-3 mēneši pirms ārstēšanas uzsākšanas ar Gilenya. Lai pārietu no teriflunomīda, ārsts var ieteikt pagaidīt noteiktu laiku vai turpināt paātrinātu eliminācijas procedūru. Ja esat ārstējies ar alemtuzumabu, rūpīgi jāizvērtē un jāapspriežas ar ārstu, lai izlemtu, vai Gilenya ir piemērots Jums.
Ja neesat pārliecināts, cik ilgi lietojat Gilenya, jautājiet savam ārstam vai farmaceitam.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Gilenya
Ja esat lietojis Gilenya vairāk nekā noteikts
Ja esat lietojis pārāk daudz Gilenya kapsulu, nekavējoties informējiet par to ārstu.
Ja esat aizmirsis lietot Gilenya
Ja esat lietojis Gilenya mazāk nekā 1 mēnesi un aizmirsis lietot 1 devu visu dienu, pirms nākamās devas lietošanas konsultējieties ar ārstu. Ārsts var nolemt jūs novērot, kad lietojat nākamo devu.
Ja esat lietojis Gilenya vismaz 1 mēnesi un esat aizmirsis lietot zāles ilgāk par 2 nedēļām, pirms nākamās devas lietošanas konsultējieties ar ārstu. Ārsts var nolemt jūs novērot, kad lietojat nākamo devu. Tomēr, ja esat aizmirsis lietot zāles 2 nedēļas vai mazāk, nākamo devu varat lietot, kā plānots.
Nekad nelietojiet dubultu devu, lai aizvietotu aizmirsto devu.
Ja pārtraucat lietot Gilenya
Nepārtrauciet Gilenya lietošanu un nemainiet devu, iepriekš nekonsultējoties ar ārstu.
Gilenya paliks organismā līdz 2 mēnešiem pēc ārstēšanas pārtraukšanas. Šajā laikā balto asins šūnu (limfocītu) skaits var palikt zems, un šajā lietošanas instrukcijā aprakstītās blakusparādības joprojām var rasties. Pēc Gilenya terapijas pārtraukšanas var būt jāgaida 6–8 nedēļas, pirms sākt jaunu multiplās sklerozes ārstēšanu.
Ja Jums ir jāatsāk Gilenya lietošana pēc vairāk nekā 2 nedēļu ilgas ārstēšanas pārtraukšanas, ietekme uz sirdsdarbības ātrumu, kas parasti parādās ārstēšanas sākumā, var atkārtoties. Slimnīca novērošanas laikā Nesāciet Gilenya lietošanu pēc tās pārtraukšanas ilgāk par divām nedēļām bez konsultēšanās ar ārstu. ārsts.
Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam vai farmaceitam
Blakusparādības Kādas ir Gilenya blakusparādības?
Tāpat kā citas zāles, šīs zāles var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Dažas blakusparādības var būt vai kļūt nopietnas
Bieži (var skart līdz 1 no 10 cilvēkiem):
- Klepus ar flegmu, diskomforts krūtīs, drudzis (plaušu traucējumu pazīmes)
- Herpes vīrusa infekcija (Sv. Antona uguns vai herpes zoster) ar tādiem simptomiem kā pūslīši, dedzināšana, nieze vai sāpes ādā, parasti ķermeņa augšdaļā vai uz sejas. Citi simptomi var būt drudzis un vājums agrīnā stadijā infekcija, kam seko nejutīgums, nieze vai sarkani plankumi ar smagām sāpēm
- Lēna sirdsdarbība (bradikardija), neregulārs sirds ritms
Retāk (var skart līdz 1 no 100 cilvēkiem):
- Pneimonija ar tādiem simptomiem kā drudzis, klepus, apgrūtināta elpošana
- Makulas tūska (pietūkums tīklenes centrālās redzes zonā acs aizmugurē) ar tādiem simptomiem kā ēnas vai aklas vietas redzes centrā, neskaidra redze, problēmas ar krāsu vai detaļu atšķiršanu
Reti (var skart līdz 1 no 1000 cilvēkiem):
- Sindroms, ko sauc par atgriezenisku atgriezenisku encefalopātiju. Simptomi var būt pēkšņas stipras galvassāpes, apjukums, krampji un / vai redzes traucējumi
Atsevišķi gadījumi:
- Kriptokoku infekcijas (sēnīšu infekcijas veids), ieskaitot kriptokoku meningītu ar tādiem simptomiem kā galvassāpes, kam pievienots kakla stīvums, jutība pret gaismu, slikta dūša un / vai apjukums.
Ja Jums rodas kāda no šīm blakusparādībām, nekavējoties informējiet ārstu.
Citas blakusparādības
Ļoti bieži (var skart vairāk nekā 1 no 10 cilvēkiem):
- Gripas vīrusa infekcija ar tādiem simptomiem kā nogurums, drebuļi, iekaisis kakls, locītavu vai muskuļu sāpes, drudzis
- Spiediena vai sāpju sajūta vaigos un pierē (sinusīts)
- Galvassāpes
- Caureja
- Muguras sāpes
- Asins analīzes, kas parāda augstāku aknu enzīmu līmeni
- Klepus
Bieži (var skart līdz 1 no 10 cilvēkiem):
- Cirpējēdes, "ādas sēnīšu infekcija (pityriasis versicolor)
- Reibonis
- Smagas galvassāpes, ko bieži pavada slikta dūša, vemšana un jutība pret gaismu (migrēna)
- Zems balto asins šūnu (limfocītu, leikocītu) līmenis
- Vājums
- Ādas izsitumi ar niezi, apsārtumu un dedzināšanu (ekzēma)
- Nieze
- Paaugstināts tauku (triglicerīdu) līmenis asinīs
- Matu izkrišana
- Sēkšana
- Depresija
- Neskaidra redze (skatīt arī sadaļu par "makulas tūsku". Dažas blakusparādības var būt vai kļūt nopietnas)
- Hipertensija (Gilenya var izraisīt nelielu asinsspiediena paaugstināšanos)
Retāk (var skart līdz 1 no 100 cilvēkiem):
- Zems dažu balto asins šūnu (neitrofilu) līmenis
- Nomākts garastāvoklis
Reti (var skart līdz 1 no 1000 cilvēkiem):
- Asinsvadu traucējumi
- Nervu sistēmas traucējumi
- Limfātiskās sistēmas vēzis (limfoma)
Nav zināms (biežumu nevar noteikt pēc pieejamiem datiem):
- Alerģiska reakcija un izsitumi uz ādas
Ja kāda no šīm blakusparādībām izpaužas smagi, lūdzu, pastāstiet to ārstam.
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu vai farmaceitu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot V pielikumā minēto valsts ziņošanas sistēmu. Ziņojot par blakusparādībām, jūs varat palīdzēt iegūt vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Uzglabāt šīs zāles bērniem neredzamā un nepieejamā vietā.
Nelietot šīs zāles pēc derīguma termiņa beigām, kas norādīts uz kastītes un blistera pēc "EXP" / "EXP". Derīguma termiņš attiecas uz norādītā mēneša pēdējo dienu.
Uzglabāt temperatūrā līdz 25ºC.
Uzglabāt oriģinālajā iepakojumā, lai pasargātu zāles no mitruma.
Nelietojiet iepakojumus, kas ir bojāti vai uz kuriem ir redzamas viltošanas pazīmes.
Neizmetiet zāles kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
Ko Gilenya satur
- Aktīvā viela ir fingolimods. Katra kapsula satur 0,5 mg fingolimoda (hidrohlorīda veidā).
- Citas sastāvdaļas ir: Kapsulas saturs: magnija stearāts, mannīts. , koncentrēts amonjaka šķīdums, kālija hidroksīds, melnais dzelzs oksīds (E172), dzeltenais dzelzs oksīds (E172), titāna dioksīds (E171), dimetikons
Gilenya ārējais izskats un iepakojums
Gilenya 0,5 mg cietajām kapsulām ir necaurspīdīgs balts necaurspīdīgs korpuss un dziļi dzeltens necaurspīdīgs vāciņš. Uz galvas ir iegravēts melns uzraksts "FTY0,5mg", bet uz ķermeņa - divas dzeltenas joslas.
Gilenya ir pieejams iepakojumos, kas satur 7, 28 vai 98 kapsulas, vai vairāku iepakojumu iepakojumos, kas satur 84 kapsulas (3 iepakojumi pa 28 kapsulām). Visi iepakojuma lielumi tirgū var nebūt pieejami.
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS
GILENYA 0,5 MG CIETAS KAPSULAS
▼ Zāles, uz kurām attiecas papildu uzraudzība. Tas ļaus ātri identificēt jaunu drošības informāciju. Veselības aprūpes speciālistus lūdz ziņot par jebkādām iespējamām blakusparādībām. Informāciju par to, kā ziņot par blakusparādībām, skatīt 4.8.
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS
Katra cietā kapsula satur 0,5 mg fingolimoda (hidrohlorīda veidā).
Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA
Cieta kapsula.
16 mm kapsula ar intensīvi dzeltenu necaurspīdīgu vāciņu un baltu necaurspīdīgu korpusu; melns gravējums "FTY0,5 mg" uz galvas un divas apaļas dzeltenas joslas, kas iegravētas uz ķermeņa.
04.0 KLĪNISKĀ INFORMĀCIJA
04.1 Terapeitiskās indikācijas
Gilenya ir indicēts atsevišķi kā slimību modificējošs līdzeklis ļoti aktīvas recidivējoši remitējošas multiplās sklerozes gadījumā šādām pieaugušo pacientu grupām:
- Pacienti ar augstu slimības aktivitāti, neskatoties uz ārstēšanu ar vismaz vienu terapiju slimību modificējoša (skatīt izņēmumus un informāciju par 4.4. un 5.1. sadaļu izskalot).
Šos pacientus var definēt kā tos, kuri nav reaģējuši uz pilnīgu un adekvātu terapijas kursu (parasti vismaz vienu ārstēšanas gadu) ar vismaz vienu terapiju slimību modificējoša. Pacientiem terapijas laikā iepriekšējā gadā jābūt vismaz vienam recidīvam, un smadzeņu MRI ir jābūt vismaz 9 T2 hiperintensīviem bojājumiem vai vismaz 1 gadolīniju pastiprinošam bojājumam. nereaģējošs to var definēt arī kā pacientu, kuram salīdzinājumā ar iepriekšējo gadu ir nemainīgs vai palielināts recidīvu biežums vai kuram ir smagi recidīvi.
vai
-Pacienti ar strauji progresējošu smagu recidivējoši remitējošu multiplo sklerozi, ko raksturo divi vai vairāki invaliditāti izraisoši recidīvi viena gada laikā, un ar 1 vai vairākiem gadolīniju uzlabojošiem smadzeņu MRI bojājumiem vai ar ievērojamu T2 bojājumu slodzes pieaugumu salīdzinājumā ar iepriekšējo MRI veikts.
04.2 Devas un lietošanas veids
Ārstēšana jāsāk un jāuzrauga ārstam, kam ir pieredze multiplās sklerozes ārstēšanā.
Devas
Ieteicamā Gilenya deva ir viena 0,5 mg kapsula iekšķīgi vienu reizi dienā. Gilenya var lietot gan ēšanas laikā, gan ārpus tās.
Ieteicams veikt tādu pašu uzraudzību kā ārstēšanas sākumā pēc pirmās devas, ja ārstēšana tiek pārtraukta šādu iemeslu dēļ:
• 1 vai vairākas dienas pirmajās divās ārstēšanas nedēļās
• vairāk nekā 7 dienas trešajā un ceturtajā ārstēšanas nedēļā
• vairāk nekā 2 nedēļas pēc viena mēneša ārstēšanas.
Ja ārstēšanas pārtraukšana ir īsāka nekā aprakstīts iepriekš, ārstēšana jāturpina, ievadot nākamo devu, kā plānots (skatīt apakšpunktu 4.4).
Īpašas populācijas
Pensionāriem
Gilenya jālieto piesardzīgi 65 gadus veciem un vecākiem pacientiem, jo nav pieejami pietiekami dati par drošību un efektivitāti (skatīt 5.2. Apakšpunktu).
Pavājināta nieru darbība
Galvenajos galvenajos pētījumos par multiplo sklerozi Gilenya nav pētīts pacientiem ar nieru darbības traucējumiem. Pamatojoties uz klīniskās farmakoloģijas pētījumiem, pacientiem ar viegliem līdz smagiem nieru darbības traucējumiem deva nav jāpielāgo.
Aknu darbības traucējumi
Gilenya nedrīkst lietot pacienti ar smagiem aknu darbības traucējumiem (C klase pēc Child-Pugh) (skatīt apakšpunktu 4.3). Lai gan pacientiem ar viegliem vai vidēji smagiem aknu darbības traucējumiem devas pielāgošana nav nepieciešama, uzsākot ārstēšanu, šiem pacientiem ieteicams ievērot piesardzību (skatīt 4.4. Un 5.2. Apakšpunktu).
Cukura diabēta slimnieki
Gilenya nav pētīts pacientiem ar multiplo sklerozi un cukura diabētu. Šiem pacientiem Gilenya jālieto piesardzīgi, jo ir iespējams paaugstināts makulas tūskas risks (skatīt 4.4. Un 4.8. Apakšpunktu). Šiem pacientiem regulāri jāpārbauda oftalmoloģija, lai noteiktu makulas tūskas pazīmes.
Pediatriskā populācija
Gilenya drošība un efektivitāte 0–18 gadus veciem bērniem vēl nav noskaidrota. Pašlaik pieejamie dati ir aprakstīti 5.2. Apakšpunktā, bet ieteikumus par devām nevar sniegt.
04.3 Kontrindikācijas
- diagnosticēts imūndeficīta sindroms.
- Pacientiem, kuriem ir paaugstināts oportūnistisku infekciju risks, ieskaitot pacientus ar pavājinātu imunitāti (ieskaitot pacientus, kuri ārstēti ar vienlaicīgu imūnsupresīvu terapiju vai tiem, kuru imunitāte ir samazināta iepriekšējās terapijas laikā).
- Smagas aktīvas infekcijas, hroniskas aktīvas infekcijas (hepatīts, tuberkuloze).
- diagnosticēti aktīvi ļaundabīgi audzēji, izņemot pacientus ar bazālo šūnu ādas vēzi.
- Smagi aknu darbības traucējumi (C klase pēc Child-Pugh).
- Paaugstināta jutība pret aktīvo vielu vai jebkuru no 6.1. Apakšpunktā uzskaitītajām palīgvielām.
04.4 Īpaši brīdinājumi un piesardzība lietošanā
Bradiaritmija
Ārstēšanas uzsākšana ar Gilenya izraisa īslaicīgu sirdsdarbības ātruma samazināšanos un var būt saistīta arī ar atrioventrikulārās vadīšanas aizkavēšanos, ieskaitot atsevišķas pilnīgas, pārejošas un spontāni izzūdošas atrioventrikulārās blokādes epizodes (skatīt 4.8. Un 5.1. Apakšpunktu).
Pēc pirmās devas ievadīšanas sirdsdarbības ātruma samazināšanās sākas vienas stundas laikā un ir maksimāla pirmajās 6 stundās. Nākamajās dienās šī iedarbība pēc devas saglabājas, lai gan parasti ir mazāka, un parasti samazinās turpmākajās nedēļās Turpinot ievadīšanu, vidējais sirdsdarbības ātrums viena mēneša laikā atgriežas sākotnējā līmenī. Tomēr, īpaši pacientiem, sirdsdarbības ātrums līdz pirmā mēneša beigām var neatgriezties sākotnējā līmenī. Vadīšanas traucējumi parasti ir bijuši pārejoši un asimptomātiski. Parasti nav nepieciešama un izzuda pirmajās 24 stundās pēc ārstēšanas uzsākšanas. Ja nepieciešams, fingolimoda izraisīto sirdsdarbības ātruma samazināšanos var novērst, parenterāli ievadot atropīna vai izoprenalīna devas.
Visiem pacientiem pirms pirmās Gilenya devas un pēc 6 stundām jāveic elektrokardiogramma un asinsspiediena mērījumi. Visi pacienti jānovēro 6 stundas, lai noteiktu bradikardijas pazīmes un simptomus, mērot pulsu stundā un mērot asinsspiedienu. Šo 6 stundu laikā ieteicams pastāvīgi (reālā laikā) kontrolēt EKG.
Ja pēc lietošanas parādās bradiaritmijas simptomi, jāuzsāk atbilstošas klīniskās pacientu ārstēšanas procedūras un jāturpina uzraudzība, līdz simptomi izzūd. Ja pēc pirmās devas pacientam novērošanas laikā nepieciešama farmakoloģiska iejaukšanās, novērošana jāveic līdz nākamajam rītam slimnīcas apstākļos un jāatkārto pēc otrās Gilenya devas.
Ja pēc 6 stundām sirdsdarbības ātrums ir zemākais pēc pirmās devas (kas liek domāt, ka maksimālā farmakodinamiskā ietekme uz sirdi vēl var nebūt izpaudusies), novērošana jāturpina vismaz 2 stundas un līdz sirds ir nepieciešama arī papildu uzraudzība (vismaz līdz nākamajam rītam un jebkurā gadījumā līdz simptomu izzušanai), ja pēc 6 stundām pēc pirmās devas ievadīšanas sirdsdarbība ir sitieni minūtē vai ja elektrokardiogrammā tiek atklāts otrās pakāpes vai augstākas pakāpes atrioventrikulāra blokāde vai QTc intervāls ir ≥500 ms. Sākoties trešās pakāpes atrioventrikulārajai blokādei, jebkurā laikā ir jāpagarina arī uzraudzība (vismaz līdz nākamajam rītam).
Smagu ritma traucējumu riska dēļ Gilenya nedrīkst lietot pacienti ar II pakāpes Mobitz II pakāpi vai augstāku atrioventrikulāro blokādi, pacientiem ar slimu sinusa sindromu vai sinoatriālo blokādi, simptomātisku bradikardiju vai atkārtotu ģīboni vai pacientiem ar ievērojamu QT pagarināšanos (QTc> 470 ms (sievietēm) vai> 450 ms (vīriešiem)). Tā kā nozīmīga bradikardija var būt slikti panesama pacientiem ar zināmu išēmisku sirds slimību (ieskaitot stenokardiju), smadzeņu asinsvadu slimībām, miokarda infarktu, sastrēguma sirds mazspēju, sirdsdarbības apstāšanos, nekontrolētu hipertensiju vai smagu miega apnoja, Gilenya nedrīkst lietot šiem pacientiem. Šiem pacientiem jāapsver ārstēšana ar Gilenya tikai tad, ja paredzamais ieguvums atsver iespējamo risku; ja tiek nolemts sākt terapiju ar Gilenya, pirms ārstēšanas uzsākšanas jākonsultējas ar kardiologu, lai noteiktu vispiemērotāko uzraudzību. Ārstēšanas uzsākšanai ieteicams novērot vismaz līdz nākamajam rītam (skatīt arī apakšpunktu 4.5).
Gilenya nav pētīts pacientiem ar aritmiju, kuriem nepieciešama ārstēšana ar Ia klases (piemēram, hinidīnu, disopiramīdu) vai III klases (piemēram, amiodaronu, sotalolu) antiaritmiskiem līdzekļiem. Ia un III klases antiaritmiskie līdzekļi ir saistīti ar torsades de pointes gadījumiem pacientiem ar bradikardiju. Tā kā ārstēšanas uzsākšana ar Gilenya samazina sirdsdarbības ātrumu, Gilenya nedrīkst lietot vienlaikus ar šīm zālēm.
Pieredze ar Gilenya lietošanu pacientiem, kuri vienlaikus tiek ārstēti ar beta blokatoriem, kalcija kanālu blokatoriem, kas izraisa sirdsdarbības ātruma samazināšanos (piemēram, verapamils, diltiazems vai ivabradīns), vai ar citām zālēm, kas var samazināt sirdsdarbības ātrumu (piemēram, digoksīns, antiholīnesterāzes zāles vai pilokarpīns). Tā kā ārstēšanas uzsākšana ar Gilenya ir saistīta arī ar sirdsdarbības ātruma samazināšanos (skatīt arī 4.8. apakšpunktu Bradiaritmija), šo zāļu vienlaicīga lietošana, uzsākot Gilenya terapiju, var būt saistīta ar smagu bradikardiju un sirds blokādi. Sakarā ar iespējamo papildinošo ietekmi uz sirdsdarbību, ārstēšanu ar Gilenya nedrīkst uzsākt pacientiem, kuri saņem šīs zāles (skatīt arī apakšpunktu 4.5). Šiem pacientiem ārstēšana ar Gilenya jāapsver tikai tad, ja paredzamais ieguvums atsver iespējamo risku. Ja tiek apsvērta terapija ar Gilenya, pirms ārstēšanas uzsākšanas ieteicams konsultēties ar kardiologu, lai apsvērtu pāreju uz citām zālēm, kas neizraisa sirdsdarbības ātruma samazināšanos. Ja nav iespējams pārtraukt ārstēšanu ar šīm zālēm, jākonsultējas ar kardiologu, lai ārstēšanas sākumā definētu adekvātu uzraudzību.
Atkarībā no pārtraukuma ilguma un ārstēšanas ilguma (laiks starp ārstēšanas sākumu un tā pārtraukšanu), atsākot ārstēšanu ar Gilenya, ietekme uz sirdsdarbību un atrioventrikulāro vadīšanu var atjaunoties. Ieteicams veikt tādu pašu uzraudzību kā ārstēšanas sākumā pēc pirmās devas, ja ārstēšana tiek pārtraukta šādu iemeslu dēļ:
• 1 vai vairākas dienas pirmajās divās ārstēšanas nedēļās
• vairāk nekā 7 dienas trešajā un ceturtajā ārstēšanas nedēļā
• vairāk nekā 2 nedēļas pēc viena mēneša ārstēšanas.
Ja ārstēšanas pārtraukums ir īsāks nekā aprakstīts iepriekš, ārstēšana jāturpina, ievadot nākamo devu, kā plānots.
QT intervāls
Rūpīgā QT intervāla pētījumā, kas tika veikts ar 1,25 mg vai 2,5 mg fingolimoda devām līdzsvara stāvoklī (kad fingolimoda negatīvā hronotropā iedarbība vēl bija), ārstēšana ar fingolimodu izraisīja devas pagarināšanos. Koriģēts QT intervāls (QTc), 90% ticamības intervāla augšējā robeža ≤ 13,0 ms. Starp fingolimoda un QTc intervāla pagarināšanos netika novērota korelācija starp devu un iedarbību, ne kā absolūtā vērtība, ne kā izmaiņas salīdzinājumā ar sākotnējo.
Šo atklājumu klīniskā nozīme nav zināma. Pētījumos ar pacientiem ar multiplo sklerozi netika novērota klīniski nozīmīga QT intervāla pagarināšanās, bet pacienti, kuriem bija risks saslimt ar QT intervāla pagarināšanos, netika iekļauti klīniskajos pētījumos.
Pacientiem ar nozīmīgiem riska faktoriem, piemēram, hipokaliēmiju vai iedzimtu QT intervāla pagarināšanos, jāizvairās no zālēm, kas var pagarināt QTc intervālu.
Infekcijas
Būtiska Gilenya farmakodinamiskā iedarbība ir no devas atkarīgs perifēro limfocītu skaita samazinājums līdz 20-30% no sākotnējās vērtības. Tas ir saistīts ar atgriezenisku limfocītu sekvestrāciju limfoīdajos audos (skatīt apakšpunktu 5.1).
Pirms ārstēšanas uzsākšanas ar Gilenya jābūt pieejamai nesenai pilnai asinsanalīzei (ti, jāņem 6 mēnešu laikā pirms vai pēc iepriekšējās terapijas pārtraukšanas). Ārstēšanas laikā ieteicams arī periodiski novērtēt asins skaitu pēc 3 mēnešiem un vismaz reizi gadā, kā arī infekcijas pazīmju parādīšanās gadījumā. Ja tiek apstiprināts absolūtais limfocītu skaits zem 0,2x109 / l, ārstēšana jāpārtrauc līdz normalizējās, jo fingolimoda lietošana tika pārtraukta klīniskajos pētījumos pacientiem ar absolūto limfocītu skaitu zem 0,2x109 / l.
Pacientiem ar ilgstošām smagām infekcijām ārstēšana ar Gilenya ir jāatliek līdz atveseļošanai.
Pirms ārstēšanas uzsākšanas ar Gilenya pacientiem jānovērtē viņu imunitātes stāvoklis attiecībā uz vējbakām. Ja nav ārsta apstiprinātas vējbakas anamnēzes vai pierādījumu par pilnīgu vakcināciju pret vējbakām, pirms Gilenya terapijas uzsākšanas pacientiem ieteicams pārbaudīt antivielas pret vējbaku zoster vīrusu (VZV). Pacientiem ar negatīvu antivielu titru pirms ārstēšanas uzsākšanas ar Gilenya ieteicams veikt pilnu vakcinācijas kursu pret vējbakām (skatīt apakšpunktu 4.8).Ārstēšanas uzsākšana ar Gilenya jāatliek par 1 mēnesi, lai vakcinācija būtu pilnībā efektīva.
Gilenya ietekme uz imūnsistēmu var palielināt infekciju risku (skatīt apakšpunktu 4.8). Pacientiem, kas ārstēti ar Gilenya un kuriem ir infekcijas simptomi, jāievieš efektīvas diagnostikas un terapeitiskās stratēģijas. Pacientiem jāinformē, ka Gilenya terapijas laikā jāpaziņo ārstam par infekcijas simptomiem.
Ja pacientam attīstās smaga infekcija, pirms ārstēšanas atsākšanas jāapsver Gilenya terapijas pārtraukšana un jānovērtē ieguvuma un riska attiecība.
Fingolimoda eliminācija pēc terapijas pārtraukšanas var ilgt līdz diviem mēnešiem, un tāpēc šajā periodā ir jāturpina infekcijas kontrole. Pacienti jābrīdina ziņot par infekcijas simptomiem divu mēnešu laikā pēc fingolimoda lietošanas pārtraukšanas.
Makulas tūska
Par makulas tūsku ar redzes traucējumiem vai bez tiem ziņots 0,5% pacientu, kuri tika ārstēti ar 0,5 mg fingolimoda, galvenokārt pirmajos 3-4 terapijas mēnešos (skatīt 4.8. Apakšpunktu). Tādēļ ir ieteicams veikt oftalmoloģisku novērtējumu 3-4 mēnešus pēc ārstēšanas sākuma.Ja pacienti jebkurā ārstēšanas laikā ziņo par redzes traucējumiem, jāveic fundūza pārbaude, ieskaitot makulas.
Pacientiem ar uveītu anamnēzē un pacientiem ar cukura diabētu ir paaugstināts makulas tūskas attīstības risks (skatīt apakšpunktu 4.8). Gilenya nav pētīts pacientiem ar multiplo sklerozi un vienlaikus cukura diabētu. Pacientiem ar multiplo sklerozi un vienlaicīgu cukura diabētu vai ar uveītu anamnēzē pirms terapijas uzsākšanas ieteicams veikt oftalmoloģisku novērtējumu un turpmākas pārbaudes ārstēšanas laikā.
Gilenya terapijas turpināšana pacientiem ar makulas tūsku nav pētīta. Ja pacientam rodas makulas tūska, ārstēšanu ar Gilenya ieteicams pārtraukt. Izlemjot, vai Gilenya terapiju atsākt pēc dziedināšanas, jāapsver iespējamais ieguvums un risks atsevišķam pacientam.
Aknu darbība
Pacientiem ar multiplo sklerozi, kas ārstēti ar Gilenya, ziņots par aknu enzīmu, īpaši alanīna aminotransferāzes (ALAT), bet arī gamma glutamiltranspeptidāzes (GGT) un aspartātransamināzes (ASAT), paaugstināšanos. Klīniskajos pētījumos ALAT līmeņa paaugstināšanās ≥ 3 reizes pārsniedz normas augšējo robežu (NPL) 8,0% pacientu, kuri tika ārstēti ar 0,5 mg fingolimoda, salīdzinot ar 1,9% pacientu, kuri tika ārstēti ar placebo. radās 1,8% pacientu, kuri tika ārstēti ar fingolimodu, un 0,9% pacientu, kuri tika ārstēti ar placebo.Klīniskos pētījumos ārstēšana ar fingolimodu tika pārtraukta, ja pieaugums bija> 5 reizes lielāks par normas augšējo robežu. Dažiem pacientiem, kuri pēc ārstēšanas pārtraukšanas tika atkārtoti ārstēti, atkārtojās aknu transamināžu līmeņa paaugstināšanās, apstiprinot saistību starp šo pieaugumu un zāļu lietošanu. Klīniskajos pētījumos aknu transamināžu līmeņa paaugstināšanās tika novērota jebkurā ārstēšanas laikā, lai gan lielākā daļa parādījās pirmajos 12 mēnešos. Asins transamināžu līmenis normalizējās aptuveni 2 mēnešus pēc fingolimoda lietošanas pārtraukšanas.
Gilenya nav pētīts pacientiem ar jau esošiem smagiem aknu darbības traucējumiem (C klase pēc Child-Pugh), tādēļ to nedrīkst lietot šiem pacientiem (skatīt apakšpunktu 4.3).
Fingolimoda imūnsupresīvo īpašību dēļ pacientiem ar aktīvu vīrusu hepatītu ārstēšanas uzsākšana jāatliek līdz aktīvās fāzes izzušanai.
Pirms ārstēšanas uzsākšanas ar Gilenya jābūt pieejamai nesenai (piemēram, pēdējo 6 mēnešu laikā) transamināžu un bilirubīna līmeņa analīzei. Ja nav klīnisku simptomu, aknu transamināžu līmenis jāpārbauda pēc 1, 3, 6, 9 un 12 mēnešiem ārstēšanas laikā un periodiski arī pēc tam. Ja aknu transamināžu līmenis sasniedz vērtības, kas pārsniedz piecas reizes vairāk nekā normas robežu (ULN), jāorganizē biežākas pārbaudes, tostarp bilirubīna un sārmainās fosfatāzes (ALP) seruma pārbaudes Ja pēc atkārtotām pārbaudēm aknas ja transamināžu vērtības ir vairāk nekā piecas reizes lielākas par normu (ULN), ārstēšana ar Gilenya jāpārtrauc un jāsāk tikai tad, kad aknu transamināžu līmenis ir normalizējies.
Pacientiem, kuriem ir aknu darbības traucējumu simptomi, piemēram, neizskaidrojama slikta dūša, vemšana, sāpes vēderā, nogurums, anoreksija, dzelte un / vai tumšs urīns, jānovērtē aknu enzīmu līmenis; ja tiek apstiprināts nozīmīgs aknu bojājums (piemēram, aknu transamināžu līmenis pārsniedz normas augšējo robežu vairāk nekā 5 reizes un / vai paaugstinās bilirubīna līmenis serumā), ārstēšana ar Gilenya jāpārtrauc. Terapijas atsākšana būs atkarīga no tā, vai ir identificēts cits aknu bojājuma cēlonis, un no pacienta ieguvuma terapijas atsākšanā, salīdzinot ar aknu darbības traucējumu atkārtošanās risku.
Lai gan nav datu, kas apstiprinātu, ka pacientiem ar jau esošu aknu slimību ir paaugstināts paaugstinātu aknu darbības testu risks, jāievēro piesardzība, lietojot Gilenya pacientiem ar nozīmīgu aknu slimību.
Iejaukšanās seroloģiskajos testos
Tā kā fingolimods samazina limfocītu skaitu asinīs, pārdalot tos sekundārajos limfoīdajos orgānos, to nevar izmantot, lai novērtētu ar Gilenya ārstētā pacienta limfocītu stāvokli. Laboratoriskajiem testiem, kuros izmanto cirkulējošas mononukleārās šūnas, ir nepieciešams lielāks asins daudzums, jo samazinās cirkulējošo limfocītu skaits.
Ietekme uz asinsspiedienu
Pacienti ar hipertensiju, ko nekontrolē zāles, tika izslēgti no Gilenya pirmspārdošanas klīniskajiem pētījumiem; tādēļ īpaša uzmanība jāpievērš, ja pacienti ar nekontrolētu hipertensiju tiek ārstēti ar Gilenya.
Klīniskajos pētījumos pacientiem ar multiplo sklerozi ārstēšana ar 0,5 mg fingolimoda bija saistīta ar vidējo sistoliskā asinsspiediena paaugstināšanos par aptuveni 3 mmHg un diastoliskā asinsspiediena palielināšanos par aptuveni 1 mmHg: šis pieaugums notika aptuveni mēnesi vēlāk. Divu gadu placebo kontrolētā pētījumā hipertensija kā blakusparādība tika ziņota 6,5% pacientu, kuri tika ārstēti ar Gilenya 0,5 mg, un 3,3% pacientu, kuri tika ārstēti ar placebo. Tādēļ ārstēšanas laikā ar Gilenya regulāri jāpārbauda asinsspiediens.
Ietekme uz elpošanas sistēmu
Ārstēšanas laikā ar Gilenya tika novērots neliels no devas atkarīgs piespiedu izelpas tilpuma (FEV1) un oglekļa monoksīda (Dlco) difūzijas spējas samazinājums, samazinājums, kas radās pirmajā mēnesī un saglabājās stabils ārstēšanas laikā. Gilenya jālieto piesardzīgi pacientiem ar smagiem elpošanas traucējumiem, plaušu fibrozi un hronisku obstruktīvu plaušu slimību (skatīt apakšpunktu 4.8).
Aizmugurējās atgriezeniskās encefalopātijas sindroms
Klīniskajos pētījumos un pēcreģistrācijas pieredzē, lietojot 0,5 mg devu, ziņots par retiem posteriori atgriezeniskas encefalopātijas sindroma (PRES) gadījumiem (skatīt 4.8. Apakšpunktu). Ziņotie simptomi bija pēkšņas stipras galvassāpes, slikta dūša, vemšana, garīga stāvokļa izmaiņas traucējumi un krampji. PRES simptomi parasti ir atgriezeniski, bet var progresēt līdz išēmiskam insultam vai smadzeņu asiņošanai. Novēlota diagnostika un ārstēšana var izraisīt neatgriezeniskas neiroloģiskas sekas. Ja ir aizdomas par PRES klātbūtni, ārstēšana ar Gilenya jāpārtrauc.
Iepriekšēja ārstēšana ar imūnsupresīvām vai imūnmodulējošām terapijām
Nav veikti pētījumi, lai novērtētu Gilenya efektivitāti un drošību, pārejot no teriflunomīda, dimetilfumarāta vai alemtuzumaba uz Gilenya. slimību modificējoša Gilenijā jāņem vērā citas terapijas pusperiods un darbības mehānisms, lai izvairītos no papildu ietekmes uz imūnsistēmu un vienlaikus samazinātu slimības atkārtotas aktivizēšanās risku. Ieteicams novērtēt pilnu asins analīzi pirms ārstēšanas uzsākšanas ar Gilenya, lai pārliecinātos, ka iepriekšējās terapijas izraisītā ietekme uz imūnsistēmu (piemēram, citopēnija) ir izzudusi.
Ārstēšanu ar Gilenya parasti var sākt tūlīt pēc interferona vai glatiramera acetāta terapijas pārtraukšanas.
Attiecībā uz dimetilfumarātu, periods izskalot tam jābūt pietiekamam, lai atjaunotu pietiekamu asins skaitu pirms ārstēšanas uzsākšanas ar Gilenya.
Natalizumaba eliminācijas pusperioda dēļ eliminācija parasti ilgst līdz 2-3 mēnešiem pēc ārstēšanas pārtraukšanas. Teriflumonīds arī lēnām tiek izvadīts no plazmas. Bez paātrinātas eliminācijas procedūras teriflunomīda izvadīšana no plazmas var ilgt no vairākiem mēnešiem līdz 2 gadiem. Ieteicams veikt paātrinātu eliminācijas procedūru, kā aprakstīts teriflunomīda zāļu aprakstā, vai arī izvadīšanas periods nedrīkst būt mazāks par 3,5 mēnešiem. Pārejot no natalizumaba vai teriflunomīda terapijas uz Gilenya, jāievēro piesardzība attiecībā uz iespējamo vienlaicīgo ietekmi uz imūnsistēmu.
Alemtuzumabam ir intensīva un ilgstoša imūnsupresīva iedarbība. Tā kā šo efektu patiesais ilgums nav zināms, nav ieteicams sākt ārstēšanu ar Gilenya pēc alemtuzumaba, ja vien ārstēšanas ieguvums atsevišķam pacientam nepārprotami atsver risku.
Lēmums par ilgstošas kortikosteroīdu terapijas vienlaicīgu lietošanu jāpieņem pēc rūpīgas apsvēršanas.
Vienlaicīga lietošana ar spēcīgiem CYP450 induktoriem
Fingolimodu jālieto piesardzīgi kombinācijā ar spēcīgiem CYP450 induktoriem. Asinszāli nav ieteicams lietot vienlaikus (skatīt 4.5. Apakšpunktu).
Terapijas pārtraukšana
Pamatojoties uz zāļu pussabrukšanas periodu, ja tiek pieņemts lēmums pārtraukt ārstēšanu ar Gilenya, jāatstāj 6 nedēļu intervāls bez terapijas, lai fingolimods varētu atbrīvoties no asinīm (skatīt 5.2. Apakšpunktu). normalizējas 1-2 mēnešu laikā pēc terapijas pārtraukšanas (skatīt 5.1. apakšpunktu). Citu terapiju uzsākšana šajā laika intervālā izraisa vienlaicīgu fingolimoda iedarbību. Imūnsupresīvo līdzekļu lietošana drīz pēc Gilenya lietošanas pārtraukšanas var papildus ietekmēt imūnsistēmu, tāpēc ieteicams ievērot piesardzību.
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi
Pretvēža, imūnmodulējošas vai imūnsupresīvas terapijas
Antineoplastisko, imūnmodulējošo vai imūnsupresīvo terapiju nedrīkst lietot vienlaikus, jo pastāv papildu ietekmes uz imūnsistēmu risks (skatīt 4.3. Un 4.4. Apakšpunktu).
Jāievēro piesardzība arī tad, ja pacienti uzsāk Gilenya terapiju pēc ilgstošas terapijas pārtraukšanas, kas ietekmē imūnsistēmu, piemēram, natalizumabu vai mitoksantronu (skatīt apakšpunktu 4.4). Klīniskajos pētījumos par sklerozi. kortikosteroīdu lietošana nebija saistīta ar paaugstinātu infekciju biežumu.
Vakcinācijas
Vakcinācija var būt mazāk efektīva ārstēšanas laikā un līdz diviem mēnešiem pēc ārstēšanas ar Gilenya pārtraukšanas. Dzīvu novājinātu vakcīnu lietošana var radīt infekciju risku, tāpēc no tās jāizvairās (skatīt 4.4. Un 4.8. Apakšpunktu).
Vielas, kas izraisa bradikardiju
Fingolimodu pētīja kombinācijā ar atenololu un diltiazēmu. Lietojot fingolimodu kopā ar atenololu mijiedarbības pētījumā ar veseliem brīvprātīgajiem, terapijas sākumā sirdsdarbības ātrums samazinājās vēl par 15%; šis efekts netika novērots, lietojot diltiazēmu. Iespējamās aditīvās iedarbības dēļ. Sirdsdarbība, ārstēšana ar Gilenya nedrīkst uzsākt pacientiem, kuri lieto beta blokatorus vai citas zāles, kas var samazināt sirdsdarbības ātrumu, piemēram, Ia un III klases antiaritmiskie līdzekļi, kalcija kanālu blokatori (piemēram, ivabradīns, verapamils vai diltiazems), digoksīns, antiholīnesterāzes vai pilokarpīns (skatīt 4.4. un 4.8. apakšpunktu). Ja šiem pacientiem tiek apsvērta ārstēšana ar Gilenya, jākonsultējas ar kardiologu, lai apsvērtu pāreju uz citām zālēm, kas neizraisa sirdsdarbības ātruma samazināšanos, vai lai noteiktu atbilstošu uzraudzību ārstēšanas sākumā. Ja nav iespējams pārtraukt ārstēšanu ar zālēm, kas samazina sirdsdarbības ātrumu, ieteicams uzraudzīt vismaz līdz nākamajam rītam.
Citu vielu izraisītas fingolimoda farmakokinētikas izmaiņas
Fingolimodu galvenokārt metabolizē CYP4F2. Citi fermenti, piemēram, CYP3A4, var būt iesaistīti arī tā metabolismā, īpaši spēcīgas CYP3A4 indukcijas gadījumā. Nav paredzams, ka spēcīgi nesējproteīna inhibitori ietekmēs fingolimoda uzvedību. Vienlaicīgi lietojot fingolimodu ar ketokonazolu, inhibējot CYP4F2, fingolimoda un fingolimoda fosfāta iedarbība (AUC) palielinājās 1,7 reizes.Lietojot fingolimodu kopā ar vielām, kas var inhibēt CYP3A4 (proteāzes inhibitori, azola pretsēnīšu līdzekļi, daži makrolīdi, piemēram, klaritromicīns vai telitromicīns), jāievēro piesardzība.
Vienlaicīga 600 mg karbamazepīna lietošana divas reizes dienā sasniedza līdzsvara stāvokli, un viena 2 mg fingolimoda deva samazināja fingolimoda un tā metabolīta AUC par aptuveni 40%. Citi spēcīgi CYP3A4 enzīma induktori, piemēram, rifampicīns, fenobarbitāls, fenitoīns, efavirenzs un asinszāle var izraisīt fingolimoda un tā metabolīta AUC samazināšanos vismaz par šo lielumu. Tā kā tas varētu mazināt to efektivitāti, jāievēro piesardzība, lietojot kombinācijā, tomēr vienlaicīga lietošana ar asinszāli nav ieteicama (skatīt apakšpunktu 4.4).
Izmaiņas citu vielu farmakoloģijā, ko izraisa fingolimods
Maz ticams, ka fingolimods mijiedarbotos ar vielām, kuras galvenokārt metabolizē CYP450 enzīmi vai galveno nesēju proteīnu substrāti.
Fingolimoda un ciklosporīna vienlaicīga lietošana neizmainīja ciklosporīna vai fingolimoda iedarbību, tāpēc nav paredzams, ka fingolimods izmainīs to zāļu farmakokinētiku, kas ir CYP3A4 substrāti.
Fingolimoda vienlaicīga lietošana ar perorālajiem kontracepcijas līdzekļiem (etinilestradiolu un levonorgestrelu) neizmainīja perorālo kontracepcijas līdzekļu iedarbību.
04.6 Grūtniecība un zīdīšana
Sievietes reproduktīvā vecumā / Kontracepcija sievietēm
Pirms ārstēšanas uzsākšanas ar Gilenya sievietes reproduktīvā vecumā jāinformē par iespējamo nopietno risku auglim un par nepieciešamību ārstēšanas laikā ar Gilenya izmantot efektīvus kontracepcijas līdzekļus. Tā kā pēc ārstēšanas pārtraukšanas ir nepieciešami apmēram divi mēneši, lai fingolimods atbrīvotos no organisma (skatīt 4.4. Apakšpunktu), iespējamais risks auglim var pastāvēt, un tāpēc kontracepcijas pasākumi jāturpina šajā laikā.
Grūtniecība
Pirms ārstēšanas uzsākšanas reproduktīvā vecuma sievietēm jābūt pieejamam negatīvam grūtniecības testam. Ārstēšanas laikā sievietēm nedrīkst iestāties grūtniecība, un ieteicama efektīva kontracepcija. Ja sieviete Gilenya lietošanas laikā iestājas grūtniecība, ārstēšanu ieteicams pārtraukt.
Pētījumi ar dzīvniekiem ir parādījuši reproduktīvo toksicitāti, tostarp augļa zudumu un orgānu defektus, īpaši noturīgus artēriju stumbra un kambaru starpsienas defektus (skatīt 5.3. Apakšpunktu). Turklāt receptors, uz kuru iedarbojas fingolimods (sfingozīna 1-fosfāts), ir iesaistīts asinsvadu veidošanā embrioģenēzes laikā. Dati par fingolimoda lietošanu grūtniecēm ir ļoti ierobežoti.
Nav datu par fingolimoda ietekmi uz dzemdībām un dzemdībām.
Barošanas laiks
Fingolimods izdalās mātes pienā laktējošiem dzīvniekiem koncentrācijā, kas ir 2–3 reizes lielāka nekā mātes plazmā (skatīt 5.3. Apakšpunktu). Tā kā iespējamas nopietnas fingolimoda blakusparādības zīdaiņiem, sievietes, kuras ārstējas ar Gilenya, nedrīkst baro bērnu ar krūti.
Auglība
Preklīnisko pētījumu dati neliecina, ka fingolimods būtu saistīts ar paaugstinātu auglības traucējumu risku (skatīt apakšpunktu 5.3).
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
Gilenya neietekmē vai nedaudz ietekmē spēju vadīt transportlīdzekļus vai apkalpot mehānismus.
Tomēr dažreiz, uzsākot ārstēšanu ar Gilenya, var rasties reibonis vai miegainība.Sākot ārstēšanu ar Gilenya, pacientus ieteicams novērot 6 stundas (skatīt apakšpunktu 4.4 Bradiaritmija).
04.8 Nevēlamās blakusparādības
Drošības profila kopsavilkums
Drošības populācija Gilenya ir iegūta no diviem III fāzes placebo kontrolētiem klīniskiem pētījumiem un viena aktīva kontrolēta III fāzes klīniska pētījuma, kas veikts pacientiem ar recidivējoši remitējošu multiplo sklerozi. Tajā kopumā ir iekļauti 2431 pacients, kas ārstēti ar Gilenya (0,5 vai 1,25 mg). Divu gadu placebo kontrolētā klīniskajā pētījumā D2301 (FREEDOMS) 854 pacienti (placebo: 418 pacienti) tika ārstēti ar fingolimodu. Divu gadu placebo kontrolētā pētījumā D2309 (FREEDOMS II) 728 pacienti ar multiplo sklerozi (placebo: 355 pacienti) tika ārstēti ar fingolimodu. Šo divu pētījumu apkopotie rezultāti liecina, ka visnopietnākās blakusparādības, kas radušās, lietojot Gilenya 0,5 mg, bija infekcijas, makulas tūska un pārejoša atrioventrikulāra blokāde ārstēšanas sākumā. Visbiežāk novērotās blakusparādības (sastopamība ≥ 10%), kas radušās, lietojot Gilenya 0,5 mg bija gripa, sinusīts, galvassāpes, caureja, muguras sāpes, paaugstināts aknu enzīmu līmenis un klepus. Visbiežāk novērotā blakusparādība, lietojot Gilenya 0,5 mg, izraisīja ārstēšanas pārtraukšanu, bija paaugstināts ALAT līmenis asinīs (2,2%). D2302 (TRANSFORMS), kurā piedalījās 849 pacienti, kuri tika ārstēti ar fingolimodu un kontrolē izmantoja beta-1α interferonu, radušās nevēlamās blakusparādības parasti bija līdzīgas tām, kas tika novērotas placebo kontrolētos pētījumos, ņemot vērā atšķirīgo pētījuma ilgumu.
Tālāk ir uzskaitītas blakusparādības, par kurām ziņots, lietojot Gilenya 0,5 mg pētījumos D2301 (BRĪVĪBAS) un D2309 (BRĪVĪBAS II). Biežuma kategorijas ir definētas, izmantojot šādu iedalījumu: ļoti bieži (≥1 / 10); bieži (≥ 1/100,
Nevēlamo blakusparādību kopsavilkuma tabula
* Nav ziņots FREEDOMS, FREEDOMS II un TRANSFORMS pētījumos. Notikumu biežuma kategorizēšana balstījās uz aprēķināto "fingolimoda iedarbību aptuveni 10 000 pacientu visos klīniskajos pētījumos".
Dažu specifisku blakusparādību apraksts
Infekcijas
Klīniskajos pētījumos pacientiem ar multiplo sklerozi kopējais infekciju biežums (65,1%), par ko ziņots, lietojot 0,5 mg devu, bija līdzīgs tam, kāds tika novērots, lietojot placebo. Tomēr ar Gilenya ārstētiem pacientiem biežāk tika novērotas apakšējo elpceļu infekcijas, galvenokārt bronhīts un, mazākā mērā, herpes infekcijas un pneimonija.
Ir ziņots par dažiem izplatītas herpes infekcijas gadījumiem, ieskaitot letālus gadījumus, pat lietojot 0,5 mg devu.
Makulas tūska
Klīniskajos pētījumos pacientiem ar multiplo sklerozi makulas tūska radās 0,5% pacientu, kuri tika ārstēti ar ieteicamo 0,5 mg devu, un 1,1% pacientu, kuri tika ārstēti ar lielāku devu (1, 25 mg). Vairums gadījumu radās pirmajos 3-4 terapijas mēnešos. Daži pacienti ziņoja par neskaidru redzi un redzes asuma samazināšanos; citi bija asimptomātiski, un diagnoze tika veikta regulāras oftalmoloģiskās vizītes laikā. Makulas tūska parasti uzlabojās vai izzuda spontāni pēc ārstēšanas pārtraukšanas. Atkārtošanās risks pēc atkārtotas ārstēšanas nav pētīts .
Makulas tūskas biežums ir palielināts pacientiem ar multiplo sklerozi, kuriem anamnēzē ir uveīts (17% ar uveītu anamnēzē, salīdzinot ar 0,6% bez uveīta). Gilenya nav pētīts pacientiem ar multiplo sklerozi un cukura diabētu. slimība, kas saistīta ar paaugstinātu makulas tūskas risku (skatīt 4.4. apakšpunktu). Klīniskajos pētījumos pacientiem ar nieru transplantātu, ieskaitot pacientus ar cukura diabētu, ārstēšana ar 2,5 mg un 5 mg fingolimoda izraisīja divreiz lielāku makulas tūskas sastopamību.
Bradiaritmija
Ārstēšanas uzsākšana ar Gilenya izraisa īslaicīgu sirdsdarbības ātruma samazināšanos un var būt saistīta arī ar atrioventrikulārās vadīšanas aizkavēšanos. Klīniskajos pētījumos pacientiem ar multiplo sklerozi maksimālais sirdsdarbības ātruma samazinājums tika novērots pirmajās 6 stundās pēc operācijas. " ārstēšanas uzsākšanas, un ārstēšanas laikā ar Gilenya 0,5 mg biežums samazinās vidēji par 12-13 sitieniem minūtē. Pacientiem, kuri tika ārstēti ar Gilenya 0,5 mg, reti tika novērota sirdsdarbības ātruma samazināšanās zem 40 sitieniem minūtē. Vidējais sirdsdarbības ātrums atgriezās sākotnējā līmenī 1 mēneša laikā pēc ārstēšanas turpināšanas. Bradikardija parasti bija asimptomātiska, taču dažiem pacientiem bija viegli vai vidēji smagi simptomi, tostarp hipotensija, reibonis, nogurums un / vai sirdsklauves, kas izzuda pirmo 24 stundu laikā pēc ārstēšanas uzsākšanas (skatīt arī 4.4. Un 5.1. Apakšpunktu).
Klīniskajos pētījumos pacientiem ar multiplo sklerozi pirmās pakāpes atrioventrikulārā blokāde ("PR intervāla pagarināšanās līdz EKG") tika novērota 4,7% pacientu, kuri tika ārstēti ar 0,5 mg fingolimoda, un 2,8% pacientu, kuri tika ārstēti ar intramuskulāru beta interferonu. 1α un 1,6% pacientu, kuri tika ārstēti ar placebo. Par otrās pakāpes atrioventrikulāro blokādi ziņots mazāk nekā 0,2% pacientu, kas ārstēti ar Gilenya 0,5 mg. Pēcreģistrācijas periodā 6 stundu novērošanas periodā pēc pirmās Gilenya devas tika ziņots par atsevišķām pārejošas, spontāni izzudušas pilnīgas atrioventrikulārās blokādes epizodēm. Pēcreģistrācijas pieredze parasti bija pārejoša, asimptomātiska un izzuda pirmo 24 dienu laikā. Lai gan vairumam pacientu nebija nepieciešama medicīniska iejaukšanās, vienam pacientam, kurš tika ārstēts ar Gilenya 0, 5 mg, tika ievadīts izoprenalīns pēc asimptomātiskas otrās pakāpes 1. tipa Mobitz atrioventrikulārās blokādes.
Pēcreģistrācijas pieredzē 24 stundu laikā pēc pirmās devas ievadīšanas ir notikuši atsevišķi notikumi ar novēlotu parādīšanos, ieskaitot pārejošu asistolu un neizskaidrojamu nāvi. Šo gadījumu novērtēšanu sarežģī vienlaicīgu zāļu un / vai jau esošu medicīnisku klātbūtne. Šo notikumu korelācija ar Gileniju ir neskaidra.
Asinsspiediens
Klīniskajos pētījumos pacientiem ar multiplo sklerozi ārstēšana ar Gilenya 0,5 mg bija saistīta ar vidējo sistoliskā asinsspiediena paaugstināšanos par aptuveni 3 mmHg un diastolisko asinsspiedienu aptuveni par 1 mmHg: šie pieaugumi notika aptuveni mēnesi vēlāk. Turpinājās ārstēšana. Par hipertensiju ziņots 6,5% pacientu, kuri tika ārstēti ar 0,5 mg fingolimoda, un 3,3% pacientu, kuri tika ārstēti ar placebo. Pirmā mēneša laikā un par pirmajā ārstēšanas dienā (skatīt arī apakšpunktu 4.4 Ietekme uz asinsspiedienu).
Aknu darbība
Ir ziņots par aknu enzīmu līmeņa paaugstināšanos pacientiem ar multiplo sklerozi, kas ārstēti ar Gilenya. Klīniskajos pētījumos asimptomātisku ALAT līmeņa paaugstināšanos asinīs ≥ 3 reizes un ≥ 5 reizes virs normas augšējās robežas (NPL) novēroja attiecīgi 8,0% un 1,8% ar Gilenya ārstēto pacientu. 0,5 mg. Dažiem pacientiem pēc ārstēšanas pārtraukšanas atkārtojās aknu transamināžu līmeņa paaugstināšanās, apstiprinot saistību starp šo pieaugumu un zālēm. Klīniskajos pētījumos aknu transamināžu līmeņa paaugstināšanās parādījās jebkurā ārstēšanas laikā, lai gan lielākā daļa parādījās pirmajos 12 mēnešos. ALAT līmenis normalizējās aptuveni 2 mēnešus pēc ārstēšanas ar Gilenya pārtraukšanas. Nelielam skaitam pacientu (N = 10, lietojot 1,25 mg devu, N = 2, lietojot 0,5 mg devu), kuriem bija ALAT līmeņa paaugstināšanās ≥ 5 reizes virs normas augšējās robežas un kuri turpināja terapiju ar Gilenya, ALAT vērtības normalizējās aptuveni 5 mēnešu laikā (skatīt arī apakšpunktu 4.4 Aknu darbība).
Nervu sistēmas traucējumi
Klīniskajos pētījumos reti gadījumi, kas saistīti ar nervu sistēmu, ieskaitot išēmisku un hemorāģisku insultu un netipiskus neiroloģiskus traucējumus, piemēram, piemēram, notikumi, kas līdzīgi akūtam izplatītam encefalomielītam (EAD).
Asinsvadu patoloģijas
Retos gadījumos perifēro artēriju slimība novērota pacientiem, kuri tika ārstēti ar fingolimodu lielākās devās (1,25 mg).
Elpošanas sistēmas
Ārstēšanas laikā ar Gilenya tika novērots neliels no devas atkarīgs piespiedu izelpas tilpuma (FEV1) un oglekļa monoksīda (Dlco) difūzijas spējas samazinājums, samazinājums, kas radās pirmajā mēnesī un saglabājās stabils ārstēšanas laikā. 24. mēnesī prognozētā FEV1 procentuālā samazināšanās, salīdzinot ar sākotnējo rādītāju, bija 0,5 mg fingolimoda un 2,7% placebo grupā, atšķirība izzuda pēc ārstēšanas pārtraukšanas. Dlco samazinājums 24. mēnesī bija 3,3%, lietojot 0,5 mg fingolimoda un 2,7% par placebo.
Limfomas
Gan klīniskajos pētījumos, gan pēcreģistrācijas periodā ir ziņots par dažāda veida limfomas gadījumiem, tostarp letālu Epšteina-Barra vīrusa (EBV) pozitīvas B šūnu limfomas gadījumu. ) klīniskajos pētījumos bija augstāks nekā gaidīts vispārējā populācijā.
Hemofagocītu sindroms
Ir ziņots par ļoti retiem hemofagocītiskā sindroma gadījumiem (Hemofagocītu sindroms, HPS) ar letālu iznākumu pacientiem, kas ārstēti ar fingolimodu "infekcijas" kontekstā. HPS ir rets stāvoklis, kas aprakstīts saistībā ar infekcijām, imūnsupresiju un dažādām autoimūnām slimībām.
Ziņošana par iespējamām blakusparādībām
Ir svarīgi ziņot par iespējamām blakusparādībām, kas radušās pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālistus lūdz ziņot par visām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu. .
04.9 Pārdozēšana
Veseliem brīvprātīgajiem vienreizējas devas, kas līdz pat 80 reizēm pārsniedza ieteicamo devu (0,5 mg), bija labi panesamas. Lietojot 40 mg devu, 5 no 6 pacientiem ziņoja par vāju spiedienu krūtīs vai savārgumu, kas klīniski saistīts ar elpceļu reaktivitāti.
Fingolimods terapijas sākumā var izraisīt bradikardiju.Sirdsdarbības ātruma samazināšanās parasti notiek vienas stundas laikā pēc pirmās devas un maksimāli pirmajās 6 stundās. Gilenya negatīvais hronotropiskais efekts saglabājas ilgāk par 6 stundām un pakāpeniski samazinās turpmākajās ārstēšanas dienās (sīkāku informāciju skatīt 4.4. Apakšpunktā). Ir ziņojumi par atrioventrikulārās vadīšanas palēnināšanos, atsevišķi ziņojumi par atrioventrikulāro blokādi. Pilnīga, pārejoša un spontāna izzušana (skatīt 4.4. un 4.8. apakšpunktu).
Ja pārdozēšana sakrīt ar pirmo Gilenya iedarbību, ir svarīgi, lai pacients vismaz pirmo 6 stundu laikā pastāvīgi (reālā laikā) kontrolētu elektrokardiogrāfiju, mērot sirdsdarbības ātrumu un asinsspiedienu (skatīt apakšpunktu 4.4).
Nepieciešama arī papildu uzraudzība (vismaz līdz nākamajam rītam un jebkurā gadījumā līdz simptomu izzušanai), ja pēc 6 stundām pēc pirmās devas ievadīšanas sirdsdarbība ir
Fingolimods netiek izvadīts ne ar dialīzi, ne ar plazmasferēzi.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS
05.1 Farmakodinamiskās īpašības
Farmakoterapeitiskā grupa: selektīvi imūnsupresanti.
ATĶ kods: L04AA27.
Darbības mehānisms
Fingolimods ir sfingozīna-1-fosfāta (S1P) receptoru modulators. Ar sfingozīnkināzes palīdzību fingolimods tiek pārveidots par aktīvo metabolītu fingolimoda fosfātu, kas zemā nanomolārā koncentrācijā saistās ar S1P1 receptoru, kas atrodas uz limfocītu virsmas, un viegli šķērso asins-smadzeņu barjeru, lai saistītos ar centrālās nervu sistēmas receptoriem sistēma S1P1, kas novietota uz centrālās nervu sistēmas šūnām. Fingolimoda fosfāts, kas darbojas kā limfocītos ekspresēto S1P receptoru funkcionāls antagonists, kavē limfocītu spēju izbēgt no limfmezgliem, kā rezultātā limfocīti tiek pārdalīti, nevis iznīcināti. Šī pārdale samazina patogēno limfocītu infiltrāciju centrālajā nervu sistēmā, kur tie ir iesaistīti nervu iekaisumos un audu bojājumos. Pētījumi ar dzīvniekiem un eksperimenti in vitro norāda, ka fingolimods var darboties arī mijiedarbojoties ar S1P receptoriem, kas izteikti uz centrālās nervu sistēmas šūnām.
Farmakodinamiskā iedarbība
4–6 stundu laikā pēc pirmās 0,5 mg fingolimoda lietošanas limfocītu skaits perifērajās asinīs samazinās līdz aptuveni 75% no sākotnējās vērtības. Turpinot ikdienas lietošanu, limfocītu skaits turpina samazināties divas nedēļas, sasniedzot minimālo vērtību aptuveni 500 šūnas / mikrolitrs jeb aptuveni 30% no sākotnējās vērtības. 18% pacientu vismaz vienu reizi sasniedza minimālo vērtību zem 200 šūnām / mikrolitrā. Ar nepārtrauktu ikdienas ārstēšanu limfocītu skaits saglabājas zems. Lielākā daļa T un B limfocītu regulāri migrē caur limfoīdiem orgāniem: fingolimods galvenokārt iedarbojas uz šīm šūnām. Apmēram 15-20% T limfocītu ir TEM (atmiņas efektora) fenotips: šīs šūnas ir svarīgas perifēro imūnsistēmas uzraudzībai. Tā kā šāda veida limfocīti parasti nemigrē uz limfoīdiem orgāniem, fingolimods neietekmē šīs šūnas. Perifēro limfocītu skaita pieaugums ir redzams dienās pēc ārstēšanas ar fingolimodu pārtraukšanas; limfocītu skaits parasti normalizējas viena līdz divu mēnešu laikā. Hroniskas fingolimoda lietošanas rezultātā nedaudz samazinās neitrofilu skaits, kas ir aptuveni 80% no sākotnējās vērtības.
Fingolimods pēc ārstēšanas uzsākšanas izraisa īslaicīgu sirdsdarbības ātruma samazināšanos un atrioventrikulārās vadīšanas samazināšanos (skatīt 4.4. Un 4.8. Apakšpunktu). Maksimālais sirdsdarbības ātruma samazinājums tiek novērots 6 stundu laikā pēc ievadīšanas, radot 70% negatīvās hronotropās iedarbības. Turpmāk ievadot, sirdsdarbība mēneša laikā atgriežas sākotnējā stāvoklī. Fingolimoda izraisīto sirdsdarbības ātruma samazināšanos var novērst, ievadot parenterāli atropīnu vai izoprenalīnu. Ir arī pierādīts, ka inhalējamam salmeterolam ir neliela pozitīva hronotropa iedarbība. Uzsākot ārstēšanu ar fingolimodu, palielinās priekšlaicīgas priekškambaru kontrakcijas, bet netiek palielināts priekškambaru mirgošanas / plandīšanās vai sirds kambaru aritmijas vai ektopija. Ārstēšana ar fingolimodu nesamazina sirdsdarbību un neietekmē sirds simpatomimētiskās reakcijas, tostarp sirdsdarbības ātruma izmaiņas dienā un reakciju uz slodzi.
Ārstēšana ar fingolimodu, vienas vai atkārtotas 0,5 mg un 1,25 mg devas divas nedēļas, neizraisa jūtamu elpceļu pretestības palielināšanos, ko mēra kā FEV1 un piespiedu izelpas plūsmu (FEF) 25-75. Tomēr, lietojot vienreizējas fingolimoda devas ≥5 mg (10 reizes lielāku par ieteicamo devu), rodas no devas atkarīgs elpceļu pretestības pieaugums. Ārstēšana ar atkārtotām 0,5 mg, 1,25 mg vai 5 mg fingolimoda devām neizraisa skābekļa pasliktināšanos vai skābekļa desaturāciju fiziskās slodzes laikā vai elpceļu atbildes reakcijas palielināšanos pret methaholīnu. Indivīdi, kas saņem fingolimodu, reaģē ar normālu bronhodilatāciju uz inhalējamiem beta-agonistiem.
Klīniskā efektivitāte un drošība
Gilenya efektivitāte tika pierādīta divos pētījumos, kuros tika novērtēta 0,5 mg un 1,25 mg fingolimoda vienreizēja lietošana pacientiem ar recidivējoši remitējošu multiplo sklerozi (RRMS). Abos pētījumos piedalījās pacienti, kuriem iepriekšējos 2 gados bija bijuši ≥ 2 recidīvi vai ≥1 recidīvs iepriekšējā gadā. Izvērstās invaliditātes statusa skalas (EDSS) rādītājs bija 0-5,5. Trešais pētījums, kas veikts tajā pašā pacientu grupā, tika pabeigts pēc Gilenijas reģistrācijas.
Divu gadu randomizētā dubultmaskētā kontrolētā placebo kontrolētā pētījumā D2301 (BRĪVĪBAS) tika iekļauti 1272 pacienti (n = 425, kas ārstēti ar 0,5 mg fingolimoda, 429 ar 1,25 mg fingolimoda, 418 ar placebo). Sākotnējo raksturlielumu vidējās vērtības bija: vecums 37 gadi, slimības ilgums 6,7 gadi, EDSS rādītājs 2,0. Rezultāti ir parādīti 1. tabulā. Nebija būtisku atšķirību starp 0,5 mg un 1,25 mg devām visiem parametriem.
1. tabula. Pētījums D2301 (BRĪVĪBAS): galvenie rezultāti
† Invaliditātes progresēšana, kas definēta kā EDSS pieaugums par 1 punktu, apstiprināta pēc 3 mēnešiem
** lpp
Visi klīniskie parametri tika novērtēti ar analīzi nodoms ārstēties. Analīzēs, kas saistītas ar MRI datiem, tika izmantotas novērtējamas datu kopas.
Pacienti, kuri bija beiguši fāzi kodols no 24 mēnešu FREEDOMS pētījuma varēja iekļūt devas aklā pagarinājuma fāzē (D2301E1) un saņemt fingolimodu. Pavisam piedalījās 920 pacienti (n = 331 turpināja lietot 0,5 mg devu, 289 - 1,25 mg devu, 155 pārgāja no placebo uz 0,5 mg un 145 no placebo uz 1,25 mg). Pēc 12 mēnešiem (36. mēnesis) 856 pacienti (93%) joprojām tika iekļauti. No 24. līdz 36. mēnesim gada recidīvu biežums (ARR) pacientiem, kuri fāzē saņēma 0,5 mg fingolimoda kodols pētījuma dalībniekiem, kuri turpināja lietot to pašu devu (0,5 mg), bija 0,17 (0,21 fāzē) kodols studiju laikā). Gadu recidīvu biežums pacientiem, kuri pārgāja no placebo uz 0,5 mg fingolimoda, bija 0,22 (0,42 fāzē) kodols studiju laikā).
Līdzīgi rezultāti tika iegūti III fāzes, 2 gadu, randomizētā, dubultmaskētā, placebo kontrolētā pētījumā (D2309; FREEDOMS 2), kurā piedalījās 1083 pacienti ar recidivējoši remitējošu multiplo sklerozi (n = 358, kuri tika ārstēti ar 0, 5 mg fingolimoda). , 370 ar fingolimodu 1,25 mg, 355 ar placebo). Sākotnējo raksturlielumu vidējās vērtības bija: vecums 41 gads, slimības ilgums 8,9 gadi, EDSS rādītājs 2,5.
2. tabula. Pētījums D2309 (BRĪVĪBAS 2): galvenie rezultāti
† Invaliditātes progresēšana, kas definēta kā EDSS pieaugums par 1 punktu, apstiprināta pēc 3 mēnešiem
** lpp
Visi klīniskie parametri tika novērtēti ar analīzi nodoms ārstēties. Analīzēs, kas saistītas ar MRI datiem, tika izmantotas novērtējamas datu kopas.
Pētījumā D2302 (TRANSFORMS) III fāze, kas ilga 1 gadu, tika randomizēta, dubultmaskēta un divkāršs manekens salīdzinājumā ar aktīvajām zālēm (beta-1α interferons) tika iekļauti 1280 pacienti (n = 429, kuri tika ārstēti ar 0,5 mg fingolimoda, 420-ar 1,25 mg fingolimoda, 431-ar intramuskulāru beta-1α injekciju 30 mikrogramu devā reizi nedēļā). Sākotnējo raksturlielumu vidējās vērtības bija: vecums 36 gadi, slimības ilgums 5,9 gadi, EDSS rādītājs 2,0. Pētījuma rezultāti ir parādīti 3. tabulā. Nebija būtiskas atšķirības starp 0,5 mg un 1,25 mg devām attiecībā uz pētījuma parametriem.
3. tabula. Pētījums D2302 (TRANSFORMS): Galvenie rezultāti
† Invaliditātes progresēšana, kas definēta kā EDSS pieaugums par 1 punktu, apstiprināta pēc 3 mēnešiem
** lpp
Visi klīniskie parametri tika novērtēti ar analīzi nodoms ārstēties. Analīzēs, kas saistītas ar MRI datiem, tika izmantotas novērtējamas datu kopas.
Pacienti, kuri bija beiguši fāzi kodols no 12 mēnešu TRANSFORMS pētījuma varēja ievadīt devas aklo pagarinājuma fāzi (D2302E1) un saņemt fingolimodu. Kopumā ieradās 1030 pacienti, tomēr 3 no viņiem nesaņēma ārstēšanu (n = 356 turpināja 0,5 mg devu, 330-1,25 mg devu, 167 no beta-1α interferona pārgāja uz 0, 5 mg un 174 no beta interferona) -1α pie 1,25 mg). Pēc 12 mēnešiem (24. mēnesis) joprojām tika iekļauti 882 pacienti (86%). No 12. līdz 24. mēnesim gada recidīvu biežums (ARR) pacientiem, kuri fāzē saņēma 0,5 mg fingolimoda kodols pētījuma dalībniekiem, kuri turpināja lietot to pašu devu (0,5 mg), bija 0,20 (0,19 fāzē) kodols studiju laikā). Gadu recidīvu biežums pacientiem, kuri pārgāja no beta-1α interferona uz 0,5 mg fingolimoda, bija 0,33 (0,48 fāzē) kodols studiju laikā).
Pētījumu D2301 un D2302 apkopotie rezultāti parādīja konsekventu un statistiski nozīmīgu samazinājumu, salīdzinot ar ikgadējā recidīvu līmeņa kontroli apakšgrupās, kuras definētas pēc dzimuma, vecuma, iepriekšējās MS terapijas, slimības aktivitātes vai invaliditātes.
Turpmāka klīnisko pētījumu rezultātu analīze parāda nozīmīgu ārstēšanas ietekmi pacientu apakšgrupās ar ļoti aktīvu recidivējoši remitējošu multiplo sklerozi.
Eiropas Zāļu aģentūra ir atlikusi pienākumu iesniegt Gilenya pētījumu rezultātus par vienu vai vairākām bērnu populācijas apakšgrupām multiplās sklerozes gadījumā (informāciju par lietošanu bērniem skatīt 4.2. Apakšpunktā).
05.2 "Farmakokinētiskās īpašības
Farmakokinētikas dati tika iegūti veseliem brīvprātīgajiem, pacientiem ar nieru transplantāciju un pacientiem ar multiplo sklerozi.
Par efektivitāti atbildīgais farmakoloģiski aktīvais metabolīts ir fingolimoda fosfāts.
Uzsūkšanās
Fingolimoda uzsūkšanās notiek lēni (Tmax 12-16 stundas) un ir plaša (≥85%). Šķietamā absolūtā biopieejamība pēc iekšķīgas lietošanas ir 93%(ticamības intervāls: 79-111%). Asins koncentrācija miera stāvoklis līmenis tiek sasniegts 1-2 mēnešu laikā pēc vienreizējas fingolimoda un allo devu lietošanas miera stāvoklis tie ir aptuveni 10 reizes lielāki nekā tie, kas novēroti, lietojot sākuma devu.
Pārtikas lietošana nemaina fingolimoda maksimālo koncentrāciju (Cmax) vai sistēmiskās iedarbības (AUC) vērtību. Fingolimoda fosfāta Cmax nedaudz palielinājās par 34%, bet AUC nemainījās, tāpēc Gilenya var lietot gan pilnā, gan tukšā dūšā (skatīt 4.2. Apakšpunktu).
Izplatīšana
Fingolimods ātri izplatās sarkanajās asins šūnās un ir 86% asins šūnu. Fingolimoda fosfātam ir par 17% zemāks sarkano asins šūnu sadalījums. Fingolimoda un fingolimoda fosfāta saistīšanās ar plazmas olbaltumvielām ir augsta (> 99%).
Fingolimods ir plaši izplatīts audos ar izkliedes tilpumu aptuveni 1200 ± 260 litri.
Biotransformācija
Cilvēkiem fingolimods tiek metabolizēts, veicot atgriezenisku stereoselektīvu fosforilāciju, veidojot fingolimoda fosfāta farmakoloģiski aktīvo (S) -enantiomēru. Fingolimods tiek izvadīts ar oksidatīvu biotransformāciju, ko galvenokārt katalizē CYP4F2 un, iespējams, citi izoenzīmi, un pēc tam sadaloties līdz neaktīviem metabolītiem, līdzīgi kā taukskābes. Tika novērota arī fingolimoda farmakoloģiski neaktīvo nepolāro keramīda analogu veidošanās. Galvenais fingolimoda metabolismā iesaistītais enzīms ir daļēji identificēts un varētu būt CYP4F2 vai CYP3A4.
Pēc vienreizējas fingolimoda [14C] iekšķīgas lietošanas galvenās ar fingolimodu saistītās sastāvdaļas, kuras asinīs tika konstatētas pēc to ietekmes uz AUC līdz 34 dienām pēc visu radioaktīvi iezīmēto sastāvdaļu ievadīšanas, ir pats fingolimods (23%), fingolimoda fosfāts ( 10%) un daži neaktīvi metabolīti (M3 karbonskābes metabolīts (8%), M29 keramīda metabolīts (9%) un M30 keramīda metabolīts (7%)).
Eliminācija
Fingolimoda klīrenss asinīs ir 6,3 ± 2,3 l / h, un vidējais terminālais eliminācijas pusperiods (t1 / 2) ir 6–9 dienas. Fingolimoda un fingolimoda fosfāta līmenis asinīs samazinās paralēli, tādējādi iegūstot līdzīgu pusi -dzīvo abām molekulām.
Pēc perorālas lietošanas aptuveni 81 % devas lēnām izdalās ar urīnu neaktīvu metabolītu veidā. Fingolimods un fingolimoda fosfāts neizvadīti neizmainītā veidā ar urīnu, bet ir kā galvenās sastāvdaļas izkārnījumos, un katrs no tiem veido mazāk nekā 2,5 % devas Pēc 34 dienām ievadītās devas atgūšana ir 89%.
Linearitāte
Fingolimoda un fingolimoda fosfāta koncentrācija acīmredzami proporcionāli palielinās pēc atkārtotas vienreizējas 0,5 mg vai 1,25 mg dienas devas ievadīšanas.
Raksturlielumi konkrētās populācijās
Fingolimoda un fingolimoda fosfāta farmakokinētika nav atšķirīga starp vīriešiem un sievietēm, pacientiem ar dažādu etnisko izcelsmi vai pacientiem ar viegliem līdz smagiem nieru darbības traucējumiem.
Personām ar viegliem, vidēji smagiem vai smagiem aknu darbības traucējumiem (A, B un C klase pēc Child-Pugh) fingolimoda Cmax izmaiņas netika novērotas, bet fingolimoda AUC palielinājās par 12%, 44%un 103%. Pacientiem ar smagiem aknu darbības traucējumiem ( C klase pēc Child-Pugh), fingolimoda fosfāta Cmax samazinājās par 22% un AUC būtiski nemainījās. Fingolimoda fosfāta farmakokinētika nav novērtēta pacientiem ar viegliem vai vidēji smagiem aknu darbības traucējumiem. Fingolimoda šķietamais eliminācijas pusperiods pacientiem ar viegliem aknu darbības traucējumiem nemainījās, bet pacientiem ar vidēji smagiem vai smagiem aknu darbības traucējumiem tas palielinājās par aptuveni 50%.
Fingolimodu nedrīkst lietot pacienti ar smagiem aknu darbības traucējumiem (C klase pēc Child-Pugh) (skatīt apakšpunktu 4.3). Fingolimoda terapija pacientiem ar viegliem un vidēji smagiem aknu darbības traucējumiem jāsāk piesardzīgi (skatīt apakšpunktu 4.2).
Klīniskā pieredze un farmakokinētikas dati par pacientiem, kas vecāki par 65 gadiem, ir ierobežoti.Gilenya jālieto piesardzīgi pacientiem no 65 gadu vecuma (skatīt apakšpunktu 4.2).
Pediatriskā populācija
Dati no nieru transplantācijas pētījuma, kurā piedalījās 7 bērni vecāki par 11 gadiem, ir ierobežoti (pētījums FTY720A0115). Šo datu salīdzināšanai ar veseliem pieaugušiem brīvprātīgajiem nav lielas nozīmes, un nevar izdarīt nozīmīgus secinājumus par fingolimoda farmakokinētiskajām īpašībām bērniem.
05.3 Preklīniskie drošības dati
Fingolimoda preklīniskais drošības profils tika novērtēts pelēm, žurkām, suņiem un pērtiķiem. Galvenie mērķa orgāni bija limfoidālā sistēma (limfopēnija un limfoīdā atrofija), plaušas (svara pieaugums, gludo muskuļu hipertrofija bronhioloalveolārajā krustojumā) un dažādām sugām sirds (negatīvs hronotropiskais efekts, paaugstināts asinsspiediens, asinis, perivaskulāras izmaiņas un miokarda). deģenerācija); 2 gadus ilgā pētījumā fingolimods iedarbojās uz asinsvadiem (vaskulopātija) tikai žurkām, lietojot 0,15 mg / kg un lielākas devas, kas aptuveni 4 reizes pārsniedz cilvēka sistēmisko iedarbību (AUC), lietojot dienas devu 0, 5. mg.
2 gadus ilgā pētījumā ar žurkām, lietojot perorālas fingolimoda devas līdz maksimālajai pieļaujamai 2,5 mg / kg devai, netika novēroti kancerogenitātes pierādījumi, kas ir aptuveni 50 reizes lielāka par cilvēka sistēmisko iedarbību (AUC), lietojot devu 0,5 mg. Tomēr 2 gadus ilgā pētījumā ar pelēm tika novērota lielāka ļaundabīgas limfomas sastopamība, lietojot 0,25 mg / kg un lielākas devas, kas atbilst aptuveni 6 reizes lielākam ekspozīcijai nekā cilvēkiem. Sistēmiskā (AUC), lietojot dienas devu 0,5 mg.
Pētījumos ar dzīvniekiem fingolimodam netika konstatēts mutagēns vai klastogēns.
Fingolimods neietekmēja žurku tēviņu un mātīšu spermatozoīdu skaitu / kustīgumu vai auglību līdz maksimālajai pārbaudītajai devai (10 mg / kg), kas ir aptuveni 150 reizes lielāka par cilvēka sistēmisko iedarbību (AUC), lietojot 0,5 dienas devu. mg.
Fingolimods, lietojot 0,1 mg / kg vai lielākas devas, žurkām ir teratogēns. Visbiežāk sastopamās augļa viscerālās anomālijas ir pastāvīgi artēriju stumbra un kambaru starpsienas defekti. Trušu teratogēno potenciālu nevar pilnībā novērtēt, tomēr palielināta embrija-augļa mirstība tika novērota, lietojot 1,5 mg / kg un lielākas devas, un samazinājās dzīvotspējīgo augļu skaits, kā arī augļa augšanas aizkavēšanās, lietojot 5 mg / kg kg.
Žurkām F1 paaudzes mazuļu izdzīvošana tika samazināta agrīnā pēcdzemdību periodā, lietojot devas, kas neizraisīja toksisku ietekmi uz mātīti. Tomēr F1 paaudzi neietekmēja ārstēšana ar fingolimodu attiecībā uz ķermeņa svaru, attīstību, uzvedību un auglību.
Fingolimods izdalījās pienā ārstētiem laktējošiem dzīvniekiem.Fingolimods un tā metabolīti grūtniecēm trušiem šķērsoja placentāro barjeru.
Vides riska novērtējums (Vides riska novērtējums, Bija)
Pacientiem ar recidivējošu multiplo sklerozi Gilenya lietošana neparedz nekādu risku videi.
06.0 FARMACEITISKĀ INFORMĀCIJA
06.1 Palīgvielas
Kapsulas saturs:
Magnija stearāts
Mannīts
Kapsulas apvalks:
Dzeltenais dzelzs oksīds (E172)
Titāna dioksīds (E171)
Želeja
Tinte:
Laka (E904)
Dehidrēts alkohols
Izopropilspirts
Butilspirts
Propilēnglikols
Attīrīts ūdens
Koncentrēts amonjaka šķīdums
Kālija hidroksīds
Melnais dzelzs oksīds (E172)
Dzeltenais dzelzs oksīds (E172)
Titāna dioksīds (E171)
Dimetikons
06.2 Nesaderība
Nav būtisks.
06.3 Derīguma termiņš
2 gadi.
06.4 Īpaši uzglabāšanas nosacījumi
Uzglabāt temperatūrā līdz 25 ° C.
Uzglabāt oriģinālajā iepakojumā, lai pasargātu zāles no mitruma.
06.5 Tiešā iepakojuma veids un iepakojuma saturs
Iepakojumi, kas satur 7, 28 vai 98 cietās kapsulas vai daudziepakojumi, kas satur 84 (3 iepakojumi pa 28) PVC / PVDC / alumīnija blisteros.
Iepakojumi, kas satur 7 x 1 cietās kapsulas perforētos blisteros ar devu / PVH / PVDH / alumīniju.
Visi iepakojuma lielumi tirgū var nebūt pieejami.
06.6 Norādījumi lietošanai un lietošanai
Nav īpašu norādījumu.
07.0 REĢISTRĀCIJAS APLIECĪBAS ĪPAŠNIEKS
Novartis Europharm Limited
Vimbblerstas ceļš
Horsham
Rietumsaseksa, RH12 5AB
Lielbritānija
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS
EU / 1/11/677 / 001-006
040949012
040949024
040949036
040949048
040949051
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS
17.03.2011
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS
2014. gada jūnijs












-cos-cause-e-sintomi-e-cura.jpg)