Aktīvās sastāvdaļas: imatinibs
Glivec 50 mg cietās kapsulas
Glivec iepakojuma ieliktņi ir pieejami šādu izmēru iepakojumiem:- Glivec 50 mg cietās kapsulas
- Glivec 100 mg cietās kapsulas
Indikācijas Kāpēc lieto Glivec? Kam tas paredzēts?
Glivec ir zāles, kas satur aktīvo vielu imatinibu. Tālāk uzskaitīto slimību gadījumā šīs zāles darbojas, kavējot patoloģisku šūnu augšanu. Tie ietver dažus vēža veidus.
Glivec ir indicēts pieaugušiem un bērniem:
- Hroniska mieloleikoze (HML). Leikēmija ir balto asins šūnu vēzis. Baltās asins šūnas parasti palīdz organismam cīnīties ar infekcijām. Hroniska mieloīdā leikēmija ir leikēmijas forma, kurā dažas patoloģiskas baltās asins šūnas (sauktas par mieloīdām šūnām) sāk nekontrolēti augt.
- Filadelfijas hromosomas pozitīva akūta limfoblastiskā leikēmija (Ph + ALL). Leikēmija ir balto asins šūnu vēzis. Baltās asins šūnas parasti palīdz organismam cīnīties ar infekcijām. Akūta limfoblastiskā leikēmija ir leikēmijas veids, kurā dažas patoloģiskas baltās asins šūnas (tā sauktie limfoblasti) sāk nekontrolēti augt. Glivec kavē šo šūnu augšanu.
Glivec ir indicēts arī pieaugušiem pacientiem, lai ārstētu:
- Mielodisplastiskas / mieloproliferatīvas slimības (MDS / MPD). Šī ir asins slimību grupa, kurā dažas asins šūnas sāk nekontrolēti augt. Glivec kavē šo šūnu augšanu noteiktos šo slimību apakštipos.
- Hipereozinofīlais sindroms (HES) un / vai hroniska eozinofīlā leikēmija (CEL). Tās ir asins slimības, kurās asins šūnas (sauktas par eozinofiliem) sāk nekontrolēti augt. Glivec kavē šo šūnu augšanu noteiktā šo slimību apakštipā.
- Ļaundabīgi kuņģa -zarnu trakta stromas audzēji (GIST). GIST ir kuņģa un zarnu audzējs, kas rodas no nekontrolētas to šūnu augšanas, kas atbalsta šo orgānu audus.
- Protubrānu dermatofibrosarkoma (DFSP). DFSP ir zemādas audu audzējs, kurā dažas šūnas sāk nekontrolēti augt. Glivec kavē šo šūnu augšanu.
Atlikušajā šīs lietošanas instrukcijas daļā, apspriežot šīs slimības, tiks izmantoti saīsinājumi.
Ja jums ir kādi jautājumi par Glivec darbību vai kāpēc jums ir parakstīts Glivec, konsultējieties ar ārstu.
Kontrindikācijas Glivec nedrīkst lietot
Glivec Jums izrakstīs tikai ārsti ar pieredzi asins vēža un cieta vēža ārstēšanā.
Uzmanīgi ievērojiet visus ārsta norādījumus, pat ja tie atšķiras no šajā lietošanas instrukcijā ietvertās vispārīgās informācijas.
Nelietojiet Glivec šādos gadījumos:
- ja Jums ir alerģija pret imatinibu vai kādu citu (6. punktā minēto) šo zāļu sastāvdaļu.
Ja tas attiecas uz jums, konsultējieties ar ārstu, nelietojot Glivec.
Ja domājat, ka Jums varētu būt alerģija, bet neesat pārliecināts, jautājiet padomu savam ārstam
Piesardzība lietošanā Kas jāzina pirms Glivec lietošanas
Pirms Glivec lietošanas konsultējieties ar ārstu:
- ja Jums ir vai kādreiz ir bijušas aknu, nieru vai sirds problēmas.
- ja lietojat levotiroksīnu, jo vairogdziedzeris ir noņemts.
Ja kaut kas no iepriekš minētā attiecas uz Jums, pirms Glivec lietošanas konsultējieties ar ārstu.
Ārstēšanas laikā ar Glivec nekavējoties pastāstiet ārstam, ja ļoti strauji pieņematies svarā. Glivec var izraisīt ķermeņa aizturi (smaga šķidruma aizture).
Glivec lietošanas laikā ārstam regulāri jāpārbauda, vai zāles ir efektīvas. Turklāt jums tiks veiktas asins analīzes un jūs regulāri nosvērsiet.
Bērni un pusaudži
Glivec ir arī līdzeklis bērniem ar HML. Nav "pieredzes par bērniem ar HML, kas jaunāki par 2 gadiem. Pieredze par bērniem ar Ph + ALL ir ierobežota, un bērnu ar MDS / MPD, DFSP, GIST un HES / CEL - ir ļoti ierobežota."
Dažiem bērniem un pusaudžiem, kuri lieto Glivec, augšana var būt lēnāka nekā parasti. Ārsts regulāri pārbaudīs augšanu.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Glivec iedarbību
Pastāstiet ārstam vai farmaceitam par visām zālēm, kuras lietojat, pēdējā laikā esat lietojis vai varētu lietot, ieskaitot zāles, ko var iegādāties bez receptes (piemēram, acetaminofēns) un augu izcelsmes zāles (piemēram, asinszāli). Dažas zāles var traucēt Glivec iedarbība, ja to lieto kopā. Tās var pastiprināt vai samazināt Glivec iedarbību, izraisot vairāk blakusparādību vai samazinot Glivec efektivitāti. Glivec var darīt to pašu ar citām zālēm.
Pastāstiet ārstam, ja lietojat zāles, kas novērš asins recekļu veidošanos.
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība. barošana ar krūti un auglība
- Ja esat grūtniece vai barojat bērnu ar krūti, ja domājat, ka Jums varētu būt grūtniecība vai plānojat grūtniecību, pirms šo zāļu lietošanas konsultējieties ar ārstu.
- Glivec nav ieteicams lietot grūtniecības laikā, ja vien tas nav absolūti nepieciešams, jo tas var kaitēt bērnam. Ārsts apspriedīs ar jums iespējamos Glivec lietošanas riskus grūtniecības laikā.
- Sievietēm, kurām var iestāties grūtniecība, ārstēšanas laikā ieteicams lietot efektīvu kontracepcijas līdzekli.
- Ārstēšanas laikā ar Glivec nedrīkst barot bērnu ar krūti.
- Pacientiem, kuri Glivec terapijas laikā ir nobažījušies par savu auglību, ieteicams konsultēties ar ārstu.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Lietojot šīs zāles, Jums var rasties reibonis vai miegainība vai redzes miglošanās. Ja tā notiek, nevadiet transportlīdzekli un nelietojiet nekādus instrumentus vai mehānismus, kamēr atkal nejūtaties labi.
Deva, lietošanas veids un laiks Kā lietot Glivec: Devas
Ārsts Jums ir izrakstījis Glivec, jo Jums ir nopietns stāvoklis. Glivec var palīdzēt jums cīnīties ar šo stāvokli.
Tomēr vienmēr lietojiet šīs zāles tieši tā, kā ārsts vai farmaceits Jums teicis.
Ir svarīgi to darīt, kamēr ārsts vai farmaceits jums to nav teicis. Ja neesat pārliecināts, jautājiet savam ārstam vai farmaceitam. Nepārtrauciet Glivec piekāršanu, ja vien ārsts to nav teicis. Ja nevarat lietot zāles, kā noteikts. apmeklējiet ārstu vai jūtat, ka jums tas vairs nav vajadzīgs, nekavējoties sazinieties ar ārstu.
Cik daudz Glivec lietot
Lietošana pieaugušajiem
Ārsts jums precīzi pateiks, cik daudz Glivec kapsulu lietot.
- Ja Jums ārstē HML:
Atkarībā no Jūsu stāvokļa parastā sākuma deva ir 400 mg vai 600 mg:
- 400 mg, kas jālieto 8 kapsulu veidā vienu reizi dienā
- 600 mg, kas jālieto kā 12 kapsulas vienu reizi dienā.
- Ja Jums ārstē GIST:
Sākuma deva ir 400 mg, kas jālieto 8 kapsulu veidā vienreiz dienā.
HML un GIST gadījumā ārsts var noteikt lielāku vai mazāku devu atkarībā no tā, kā jūs reaģējat uz ārstēšanu. Ja dienas deva ir 800 mg (16 kapsulas), jums vajadzēs lietot 8 kapsulas no rīta un 8 kapsulas vakarā. - Ja Jums ārstē Ph + ALL: Sākuma deva ir 600 mg, kas jālieto kā 12 kapsulas vienu reizi dienā. - Ja Jums ārstē MSD / MPD: Sākuma deva ir 400 mg, kas jālieto kā 8 kapsulas vienu reizi dienā. - Ja Jums ārstē HES / CLE: Sākuma deva ir 100 mg, kas jālieto kā 2 kapsulas vienu reizi dienā. Jūsu ārsts var izlemt palielināt devu līdz 400 mg, kas jālieto kā 8 kapsulas vienu reizi dienā, pamatojoties uz Jūsu atbildes reakciju uz ārstēšanu. - Ja Jums tiek ārstēta DFSP: Deva ir 800 mg dienā (16 kapsulas), kas jālieto kā 8 kapsulas no rīta un 8 kapsulas vakarā. Lietošana bērniem un pusaudžiem Ārsts jums pateiks, cik daudz Glivec kapsulu dot bērnam. Glivec ievadītais daudzums būs atkarīgs no bērna stāvokļa, viņa svara un auguma. Kopējā dienas deva nedrīkst pārsniegt 800 mg bērniem ar HML un 600 mg bērniem ar Ph + ALL. Ārstēšanu bērnam var ievadīt kā vienu dienas devu, vai arī dienas devu var sadalīt divās devās (pusi no rīta un pusi vakarā). Kad un kā lietot Glivec Cik ilgi lietot Glivec Turpiniet lietot Glivec katru dienu tik ilgi, cik noteicis ārsts. Ja esat lietojis Glivec vairāk nekā noteikts Ja nejauši esat lietojis pārāk daudz kapsulu, nekavējoties sazinieties ar savu ārstu. Jums var būt nepieciešama medicīniska palīdzība. Paņemiet līdzi zāļu kastīti. Ja esat aizmirsis lietot Glivec Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam, farmaceitam vai medmāsai. Tāpat kā citas zāles, šīs zāles var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas. Tās parasti ir vieglas vai vidēji smagas. Dažas blakusparādības var būt nopietnas. Nekavējoties pastāstiet ārstam, ja Jums rodas kāds no šiem simptomiem: Ļoti bieži (var skart vairāk nekā 1 no 10 cilvēkiem) vai bieži (var skart līdz 1 no 10 cilvēkiem): Retāk (var skart līdz 1 no 100 cilvēkiem) vai reti (var skart līdz 1 no 1000 cilvēkiem): Nav zināms (biežumu nevar noteikt pēc pieejamiem datiem): Ja Jums rodas kāda no iepriekš aprakstītajām sekām, lūdzu, nekavējoties informējiet ārstu. Citas blakusparādības var būt: Ļoti bieži (var skart vairāk nekā 1 no 10 cilvēkiem): Ja kāda no šīm blakusparādībām jūs smagi ietekmē, pastāstiet par to savam ārstam. Bieži (var skart līdz 1 no 10 cilvēkiem): Ja kāda no šīm blakusparādībām jūs smagi ietekmē, pastāstiet par to savam ārstam. Nav zināms (biežumu nevar noteikt pēc pieejamiem datiem): Ziņošana par blakusparādībām Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu, farmaceitu vai medmāsu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā lietošanas instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot V pielikumā minēto valsts ziņošanas sistēmu. sniedziet vairāk informācijas par šo zāļu drošumu. Ko Glivec satur Glivec izskata un iepakojuma saturs Glivec 50 mg kapsulas ir gaiši dzeltenā līdz dzeltenīgi oranžā krāsā un ar apzīmējumu "NVR SH". Tie satur baltu līdz dzeltenu pulveri. Tie tiek piegādāti iepakojumā pa 30 kapsulām. Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī.Pieejamā informācija var nebūt aktuāla. GLIVEC 50 MG CIETAS KAPSULAS Katra kapsula satur 50 mg imatiniba (mezilāta veidā). Pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1. Cieta kapsula Balts līdz dzeltens pulveris gaiši dzeltenā līdz dzeltenīgi oranžā necaurspīdīgā kapsulā ar uzdruku "NVR SH". Glivec ir indicēts ārstēšanai • pieaugušiem un bērniem ar nesen diagnosticētu Filadelfijas hromosomu (bcr-abl) pozitīvu (Ph +) hronisku mieloleikozi (HML), kuriem kaulu smadzeņu transplantācija netiek uzskatīta par pirmās izvēles ārstēšanu. • pieaugušiem un bērniem ar hronisku fāzes Ph + HML pēc alfa interferona terapijas neveiksmes vai paātrinātas fāzes vai blastu krīzes. • pieaugušiem un bērniem ar nesen diagnosticētu Filadelfijas hromosomu pozitīvu akūtu limfoblastisko leikēmiju (Ph + ALL), kas papildināta ar ķīmijterapiju. • pieaugušiem pacientiem ar recidivējošu vai refraktāru Ph + ALL monoterapijā. • pieaugušiem pacientiem ar mielodisplastiskām / mieloproliferatīvām slimībām (MDS / MPD), kas saistītas ar trombocītu izcelsmes augšanas faktora receptoru (PDGFR) gēna pārkārtošanos. • pieaugušiem pacientiem ar progresējošu hipereozinofīlo sindromu (HES) un / vai hronisku eozinofīlo leikēmiju (CEL) ar FIP1L1-PDGFRa pārkārtošanos. Glivec ietekme uz kaulu smadzeņu transplantācijas iznākumu nav noteikta. Glivec ir indicēts • pieaugušu pacientu ārstēšana ar neatgriezeniskiem un / vai metastātiskiem ļaundabīgiem kuņģa -zarnu trakta stromas audzējiem (GIST), Kit pozitīvs (CD 117). • adjuvanta ārstēšana pieaugušiem pacientiem ar ievērojamu recidīva risku pēc Kit pozitīvo GIST rezekcijas (CD 117). Pacientiem ar zemu vai ļoti zemu recidīvu risku nevajadzētu saņemt adjuvantu terapiju. • tādu pieaugušu pacientu ārstēšana, kuriem ir nenovēršams dermatofibrosarkomas protuberans (DFSP), un pieaugušu pacientu ar recidivējošu un / vai metastātisku DFSP, kuri nav piemēroti operācijai. Glivec efektivitāte pieaugušajiem un bērniem ir balstīta uz vispārējo hematoloģisko un citoģenētisko atbildes reakciju un dzīvildzi bez progresēšanas HML, uz hematoloģiskās un citoģenētiskās atbildes vērtībām Ph + ALL, MDS / MPD, uz hematoloģiskās atbildes vērtībām. HES / CLE un par objektīvām atbildes vērtībām pieaugušiem pacientiem ar neatgriezenisku un / vai metastātisku GIST un DFSP un izdzīvošanu bez recidīviem GIST adjuvantā ārstēšanā. Pieredze par Glivec lietošanu pacientiem ar MDS / MPD, kas saistīta ar PDGFR gēnu ierobežots (skatīt apakšpunktu 5.1). Nav kontrolētu klīnisku pētījumu, kas pierādītu klīnisko ieguvumu vai palielinātu izdzīvošanu šajos apstākļos, izņemot tos, kas veikti nesen diagnosticētas HML hroniskas fāzes gadījumā. Terapija jāuzsāk ārstam, kuram ir pieredze, ārstējot pacientus ar hematoloģiskiem audzējiem un ļaundabīgām sarkomām. Paredzētā deva jāievada iekšķīgi, ēdienreizes laikā un uzdzerot lielu glāzi ūdens, lai samazinātu kuņģa -zarnu trakta kairinājuma risku.800 mg dienā jāievada 400 mg divas reizes dienā, no rīta un vakarā. Pacientiem (bērniem), kuri nevar norīt kapsulas, saturu var atšķaidīt glāzē negāzēta ūdens vai ābolu sulas. Tā kā pētījumi ar dzīvniekiem ir parādījuši reproduktīvās toksicitātes pazīmes un iespējamais risks cilvēka auglim nav zināms, sievietēm reproduktīvā vecumā, kuras atver kapsulas, ar to saturu jārīkojas uzmanīgi un jāizvairās no saskares ar acīm vai ieelpošanas (skatīt 4.6. Apakšpunktu). mazgāt tūlīt pēc apstrādes ar atvērtām kapsulām. Devas HML pieaugušiem pacientiem Pieaugušiem pacientiem ar HML hroniskā fāzē ieteicamā Glivec deva ir 400 mg dienā. HML tiek definēts kā hronisks, ja ir izpildīti visi šie kritēriji: asinis un kaulu smadzenes uzspridzina perifēro asiņu bazofilu trombocīti> 100 x 109 / l. Paātrinātā fāzē pieaugušiem pacientiem ieteicamā Glivec deva ir 600 mg dienā. Paātrināto fāzi nosaka kāds no šiem gadījumiem: blasti asinīs vai kaulu smadzenēs ≥15%, bet Pieaugušiem pacientiem blastu krīzes gadījumā ieteicamā Glivec deva ir 600 mg dienā. Blastu krīzi nosaka asins vai kaulu smadzeņu blastu klātbūtne ≥30% vai ar ekstramedulāru slimību, kas nav hepatosplenomegālija. Ārstēšanas ilgums: Klīniskajos pētījumos Glivec terapija turpinājās līdz slimības progresēšanai. Ārstēšanas pārtraukšanas ietekme pēc pilnīgas citoģenētiskās atbildes reakcijas nav pētīta. Pacientiem ar hronisku fāzi devas var palielināt no 400 mg līdz 600 mg vai 800 mg vai pacientiem no hroniskas fāzes no 600 mg līdz maksimālajai 800 mg (ievadot 400 mg divas reizes dienā). smagu zāļu blakusparādību neesamība un smaga neitropēnija vai trombocitopēnija, kas nav saistīta ar leikēmiju šādos apstākļos: slimības progresēšana (jebkurā laikā); nespēja iegūt apmierinošu hematoloģisku atbildes reakciju pēc vismaz 3 mēnešu ārstēšanas; nespēja iegūt citoģenētisku reakciju pēc 12 ārstēšanas mēnešiem; vai iepriekš iegūtas hematoloģiskas un / vai citoģenētiskas atbildes zudums. Pacienti rūpīgi jānovēro, vai nav palielināta deva, ņemot vērā iespējamo blakusparādību biežuma palielināšanos, lietojot lielākas devas. Devas HML ārstēšanai bērniem Devas bērniem jāaprēķina, pamatojoties uz ķermeņa virsmas laukumu (mg / m2). Bērniem ar hronisku un progresējošu HML HL ieteicama dienas deva 340 mg / m2 (nepārsniegt kopējo devu 800 mg). Kopējo dienas devu var lietot kā vienu devu vai sadalīt divās devās - vienu no rīta un vienu vakarā. Devas ieteikumi pašlaik ir balstīti uz ierobežotu bērnu skaitu (skatīt 5.1. Un 5.2. Apakšpunktu). dati par ārstēšanu bērniem līdz 2 gadu vecumam. Ja nav smagu zāļu blakusparādību un smagas neitropēnijas vai trombocitopēnijas, kas nav saistīta ar leikēmiju, pediatriskā populācija var palielināt dienas devu no 340 mg / m2 līdz 570 mg / m2 (nepārsniedzot kopējo 800 mg devu). šādos apstākļos: slimības progresēšana (jebkurā laikā); nespēja sasniegt apmierinošu hematoloģisko atbildes reakciju pēc vismaz 3 ārstēšanas mēnešiem, nespēja sasniegt citoģenētisko atbildes reakciju pēc 12 ārstēšanas mēnešiem; vai iepriekš iegūto hematoloģisko un / vai Pēc devas palielināšanas pacienti rūpīgi jānovēro, ņemot vērā iespējamo blakusparādību biežuma palielināšanos, lietojot lielākas devas. Ph + ALL devas pieaugušiem pacientiem Pieaugušiem pacientiem ar Ph + ALL ieteicamā Glivec deva ir 600 mg dienā. Hematologi ekspertiem šīs slimības ārstēšanā ir jāuzrauga terapija visos ārstēšanas posmos. Ārstēšanas shēma: Pamatojoties uz esošajiem datiem, ir pierādīts, ka Glivec ir efektīvs un drošs, ja to ievada 600 mg dienā kombinācijā ar ķīmijterapiju indukcijas, konsolidācijas un uzturēšanas fāzēs (skatīt 5.1. Apakšpunktu), ko lieto pieaugušo pacientu ārstēšanai. nesen diagnosticēts Ph + ALL Glivec terapijas ilgums var atšķirties atkarībā no izvēlētās ārstēšanas shēmas, bet parasti labāki rezultāti ir sasniegti, ilgāk lietojot Glivec. Pieaugušiem pacientiem ar recidivējošu vai ugunsizturīgu Ph + ALL Glivec monoterapija 600 mg dienā ir droša, efektīva un to var ievadīt līdz slimības progresēšanai. Devas Ph + ALL ārstēšanai bērniem Devas bērniem jāaprēķina, pamatojoties uz ķermeņa virsmas laukumu (mg / m2). Bērniem ar Ph + ALL ieteicamā dienas deva ir 340 mg / m2 (nepārsniedzot kopējo devu 600 mg). MDS / MPD devas Pieaugušiem pacientiem ar MDS / MPD ieteicamā Glivec deva ir 400 mg dienā. Ārstēšanas ilgums: Vienīgajā līdz šim veiktajā klīniskajā pētījumā ārstēšana ar Glivec tika turpināta līdz slimības progresēšanai (skatīt 5.1. Apakšpunktu). Analīzes laikā vidējais ārstēšanas ilgums bija 47 mēneši (24 dienas - 60 mēneši). Devas HES / CLE Pieaugušiem pacientiem ar HES / CEL ieteicamā Glivec deva ir 100 mg dienā. Ja nav novērotas blakusparādības, var apsvērt devas palielināšanu no 100 mg līdz 400 mg, ja novērtējumi liecina par nepietiekamu terapeitisko atbildes reakciju. Ārstēšana jāturpina tik ilgi, kamēr pacients no tā gūst labumu. Devas GIST Pieaugušiem pacientiem ar neatgriezenisku un / vai metastātisku ļaundabīgu GIST ieteicamā Glivec deva ir 400 mg dienā. Ir ierobežoti dati par devas palielināšanas ietekmi no 400 mg uz 600 mg vai 800 mg pacientiem, kuri pāriet uz mazāko devu (skatīt 5.1. Apakšpunktu). Ārstēšanas ilgums: Klīniskajos pētījumos ar GIST pacientiem ārstēšana ar Glivec tika turpināta līdz slimības progresēšanai. Analīzes laikā ārstēšanas ilgums bija vidēji 7 mēneši (no 7 dienām līdz 13 mēnešiem). Nav pētīta ārstēšanas pārtraukšanas ietekme pēc atbildes reakcijas sasniegšanas. Pieaugušiem pacientiem ar GIST pēc rezekcijas ieteicamā Glivec deva adjuvanta ārstēšanai ir 400 mg dienā. Optimālais adjuvanta terapijas ilgums vēl nav noteikts. Ārstēšanas ilgums klīniskajā pētījumā, kas pamatoja šo indikāciju, bija 36 mēneši (skatīt apakšpunktu 5.1). Devas DFSP Pieaugušiem pacientiem ar DFSP ieteicamā Glivec deva ir 800 mg dienā. Devas pielāgošana blakusparādību gadījumā Nehematoloģiskas blakusparādības Ja, lietojot Glivec, rodas nevēlamas blakusparādības, ārstēšana jāpārtrauc, līdz notikums izzūd. Pēc tam ārstēšanu var atsākt pēc vajadzības atkarībā no notikuma sākotnējā smaguma pakāpes. Ja bilirubīna līmenis paaugstinās vairāk nekā 3 reizes virs institucionālās normālās augšējās robežas vai aknu transamināžu līmenis pārsniedz piecas reizes IULN robežu, Glivec lietošana jāpārtrauc tik ilgi, kamēr bilirubīna līmenis ir atgriezies zem 1,5 reizes IULN robeža un transamināžu līmenis zem 2,5 reizes pārsniedz IULN robežu. Glivec terapiju var turpināt, samazinot dienas devu. Pieaugušajiem deva jāsamazina no 400 līdz 300 mg vai no 600 līdz 400 mg vai no 800 mg līdz 600 mg un bērniem no 340 līdz 260 mg / m2 dienā. Hematoloģiskas blakusparādības Smagas neitropēnijas un trombocitopēnijas gadījumā ieteicams samazināt devu vai pārtraukt ārstēšanu, kā norādīts zemāk esošajā tabulā. Devas pielāgošana neitropēnijas un trombocitopēnijas gadījumā: Īpašas pacientu kategorijas Lietošana pediatrijā: nav pieredzes bērniem ar HML, kas jaunāki par 2 gadiem, un bērniem ar Ph + ALL, kas jaunāki par 1 gadu (skatīt 5.1. apakšpunktu). Pieredze bērniem ar MDS / MPD, DFSP, GIST un HES / LEC ļoti ierobežots. Imatiniba drošums un efektivitāte bērniem ar MDS / MPD, DFSP, GIST un HES / CEL jaunākiem par 18 gadiem nav pierādīta klīniskajos pētījumos. Pašlaik pieejamie publicētie dati ir apkopoti 5.1. Apakšpunktā, taču nevar sniegt ieteikumus par devām . Aknu mazspēja: imatinibs galvenokārt tiek metabolizēts caur aknām. Pacientiem ar viegliem, vidēji smagiem vai smagiem aknu darbības traucējumiem jāsniedz minimālā ieteicamā deva 400 mg dienā. Ja to nepanes, devu var samazināt (skatīt 4.4., 4.8. Un 5.2. Apakšpunktu). Aknu disfunkcijas klasifikācija: ULN = iestādes augšējā normas robeža AST = aspartāta aminotransferāze Nieru mazspēja: Pacientiem ar nieru darbības traucējumiem vai dialīzi sākumdeva jāsniedz minimālā ieteicamā deva 400 mg dienā. Tomēr šiem pacientiem ieteicams ievērot piesardzību. Ja to nepanes, devu var samazināt. Ja panesamību, devu var palielināt efektivitātes trūkuma dēļ (skatīt 4.4. Un 5.2. Apakšpunktu). Vecāki cilvēki: imatiniba farmakokinētika gados vecākiem cilvēkiem nav īpaši pētīta. Pieaugušiem pacientiem klīniskos pētījumos, kuros piedalījās vairāk nekā 20% pacientu vecumā no 65 gadiem, netika novērotas būtiskas ar vecumu saistītas farmakokinētikas atšķirības. Gados vecākiem cilvēkiem nav nepieciešami īpaši devu ieteikumi. Paaugstināta jutība pret aktīvo vielu vai jebkuru no 6.1. Apakšpunktā uzskaitītajām palīgvielām. Ja Glivec tiek lietots kopā ar citām zālēm, iespējama zāļu mijiedarbība. Jāievēro piesardzība, lietojot Glivec kopā ar proteāzes inhibitoriem, azola pretsēnīšu līdzekļiem, dažiem makrolīdiem (skatīt 4.5. Apakšpunktu), CYP3A4 substrātiem ar šauru terapeitisko logu (piemēram, ciklosporīnu, pimozīdu, takrolimu, sirolimu, ergotamīnu, diergotamīnu, fentanilu, alfentanilu, terfenadīnu, bortezomibu). , docetakselu, hinidīnu) vai varfarīnu un citus kumarīna atvasinājumus (skatīt 4.5. apakšpunktu). Vienlaicīga imatiniba lietošana ar zālēm, kas inducē CYP3A4 (piemēram, deksametazonu, fenitoīnu, karbamazepīnu, rifampicīnu, fenobarbitālu vaiHypericum perforatum(pazīstams arī kā asinszāle) var ievērojami samazināt Glivec iedarbību, potenciāli palielinot ārstēšanas neveiksmes risku.Tāpēc jāizvairās no vienlaicīgas spēcīgu CYP3A4 induktoru un imatiniba lietošanas (skatīt apakšpunktu 4.5). Hipotireoze Ir ziņots par klīniskiem hipotireozes gadījumiem pacientiem ar vairogdziedzera darbības traucējumiem, kuri terapijas laikā ar Glivec saņēma levotiroksīna aizstājēju (skatīt apakšpunktu 4.5). Šādiem pacientiem rūpīgi jāuzrauga vairogdziedzeri stimulējošā hormona (TSH) līmenis. Hepatotoksicitāte Glivec metabolisms galvenokārt notiek aknās, un tikai 13% ekskrēcijas notiek caur nierēm. Pacientiem ar aknu darbības traucējumiem (vieglu, vidēji smagu vai smagu) rūpīgi jāpārbauda perifēro asins analīzes un aknu enzīmi (skatīt 4.2., 4.8. Un 5.2. Apakšpunktu). ). Ir konstatēts, ka pacientiem ar GIST var būt metastāzes aknās, kas var izraisīt aknu darbības traucējumus. Lietojot imatinibu, novēroti aknu bojājumu gadījumi, tostarp aknu mazspēja un aknu nekroze. Ja imatinibu lieto kombinācijā ar lielām ķīmijterapijas shēmām, ziņots par smagu aknu reakciju pastiprināšanos. Aknu darbība rūpīgi jāuzrauga situācijās, kad imatinibs tiek kombinēts ar ķīmijterapijas shēmām, kas arī ir zināmas kā saistītas ar aknu darbības traucējumiem (skatīt 4.5. Un 4.8. Apakšpunktu). Šķidruma aizture Ir ziņots par smagiem šķidruma aiztures gadījumiem (izsvīdums pleirā, tūska, plaušu tūska, ascīts, virspusēja tūska) aptuveni 2,5% no nesen diagnosticētiem HML pacientiem, kuri ārstēti ar Glivec. Tāpēc ir ļoti ieteicams regulāri nosvērt pacientus. Negaidīts straujš svara pieaugums ir rūpīgi jāizpēta un, ja nepieciešams, jāveic atbilstoša atbalstoša aprūpe un terapeitiskie pasākumi. Klīniskajos pētījumos šo notikumu biežums ir palielinājies gados vecākiem cilvēkiem un tiem, kam anamnēzē ir sirds slimība, tādēļ pacientiem ar sirds darbības traucējumiem jāievēro piesardzība. Pacienti ar sirds slimībām Pacienti ar sirds slimībām, sirds mazspējas riska faktoriem vai nieru mazspēju anamnēzē ir rūpīgi jānovēro, un visi pacienti ar sirds vai nieru mazspējas pazīmēm vai simptomiem jānovērtē un jāārstē. Pacientiem ar hipereozinofīlo sindromu (HES) ar slēptu HES šūnu infiltrāciju miokardā atsevišķi HARD šūnu degranulācijas gadījumi drīz pēc imatiniba terapijas uzsākšanas ir saistīti ar atsevišķiem kardiogēna šoka / kreisā kambara disfunkcijas gadījumiem. Ir ziņots, ka stāvoklis ir atgriezenisks, lietojot sistēmiski steroīdus, veicot hemodinamikas atbalsta pasākumus un īslaicīgi pārtraucot imatiniba lietošanu. Tā kā ar imatinibu retāk ziņots par nevēlamām sirds parādībām, pirms ārstēšanas uzsākšanas rūpīgi jāapsver imatiniba terapijas ieguvuma un riska attiecība HES / CEL pacientu populācijā. Mielodisplastiskas / mieloproliferatīvas slimības ar PDGFR gēnu pārkārtošanos var būt saistītas ar paaugstinātu eozinofilu līmeni. Tādēļ pacientiem ar HES / CEL un pacientiem ar MDS / MPD, kas saistīts ar paaugstinātu eozinofilu līmeni, pirms imatiniba ievadīšanas jāapsver kardiologa novērtējums, ehokardiogrammas veikšana un troponīna līmeņa noteikšana serumā. Viens no diviem nav pieejams no normas, terapijas sākumā vienu līdz divas nedēļas vienlaikus ar terapijas sākšanu jāapsver periodiska kardiologa pārbaude un profilaktiska sistēmisko steroīdu (1-2 mg / kg) lietošana. Kuņģa -zarnu trakta asiņošana Pētījumā ar pacientiem ar neatgriezenisku un / vai metastātisku GIST tika ziņots gan par kuņģa-zarnu trakta, gan audzēja iekšējiem asiņojumiem (skatīt 4.8. Apakšpunktu). Pamatojoties uz pieejamajiem datiem, nav konstatēti predisponējoši faktori (piemēram, audzēja lielums, audzēja atrašanās vieta, koagulācijas izmaiņas), kas paaugstinātu abu asiņošanas veidu risku pacientiem ar GIST. Tā kā palielināta vaskularitāte un tieksme uz asiņošanu ir daļa no GIST rakstura un klīniskās gaitas, visiem pacientiem jāpieņem vispārēja medicīniskā prakse un procedūras asiņošanas uzraudzībai un ārstēšanai. Audzēja līzes sindroms Sakarā ar iespējamo audzēja līzes sindroma (TLS) rašanos, pirms Glivec lietošanas uzsākšanas ieteicams izlabot klīniski nozīmīgu dehidratāciju un ārstēt augstu urīnskābes līmeni (skatīt 4.8. Apakšpunktu). Laboratorijas analīze Glivec terapijas laikā regulāri veiciet pilnu asins analīzi. HML pacientu ārstēšana ar Glivec ir saistīta ar neitropēniju vai trombocitopēniju. Tomēr šo citopēniju rašanās, iespējams, ir saistīta ar ārstētās slimības stadiju un bija biežāka pacientiem ar CML paātrinātu fāzi vai blastu krīzi nekā pacientiem ar HML hroniskā fāzē. Ārstēšanu ar Glivec var pārtraukt vai samazināt devu, kā ieteikts 4.2. Pacientiem, kuri tiek ārstēti ar Glivec, regulāri jākontrolē aknu darbība (transamināzes, bilirubīns, sārmainā fosfatāze). Pacientiem ar nieru darbības traucējumiem imatiniba ekspozīcija plazmā, šķiet, ir lielāka nekā tā, kas novērota pacientiem ar normālu nieru darbību, iespējams, tāpēc, ka šiem pacientiem ir paaugstināts alfa skābes glikoproteīna (AGP) līmenis, proteīns, kuram imatinibs saistās. Pacientiem ar nieru darbības traucējumiem jāsniedz mazākā sākumdeva. Pacienti ar smagiem nieru darbības traucējumiem jāārstē piesardzīgi. Ja to nepanes, devu var samazināt (skatīt 4.2. Un 5.2. Apakšpunktu). Pediatriskā populācija Ir ziņots par augšanas kavēšanās gadījumiem bērniem un pusaudžiem, kuri ārstēti ar imatinibu. Ilgstošas ārstēšanas ar imatinibu ietekme uz bērnu augšanu nav zināma. Tādēļ ieteicams rūpīgi kontrolēt augšanu bērniem, kuri saņem imatinibu (skatīt apakšpunktu 4.8). Aktīvās vielas, kas var palielināt imatiniba koncentrāciju plazmā: Vielas, kas kavē citohroma P450 izoenzīma CYP3A4 aktivitāti (piemēram, proteāzes inhibitori, piemēram, indinavīrs, lopinavīrs / ritonavīrs, ritonavīrs, sakvinavīrs, telaprevīrs, nelfinavīrs, boceprevīrs; azola pretsēnīšu līdzekļi, ieskaitot ketokonazolu, itolidrakonazolu, dažus makricona, piemēram, makromikronu, piemēram, (klaritromicīns un telitromicīns) var samazināt metabolismu un palielināt imatiniba koncentrāciju. Lietojot vienlaicīgi ar vienu ketokonazola (CYP3A4 inhibitora) devu, veseliem cilvēkiem ievērojami palielinājās imatiniba iedarbība (imatiniba vidējās Cmax un AUC vērtības palielinājās attiecīgi par 26% un 40%). Lietojot Glivec kopā ar CYP3A4 inhibitoru saimes, jāievēro piesardzība. Aktīvās vielas, kas var samazināt imatiniba koncentrāciju plazmā: Vielas, kas stimulē CYP3A4 aktivitāti (piemēram, deksametazons, fenitoīns, karbamazepīns, rifampicīns, fenobarbitāls, fosfenitoīns, primidons vaiHypericum perforatum(pazīstams arī kā asinszāle) var ievērojami samazināt Glivec iedarbību, potenciāli palielinot ārstēšanas neveiksmes risku. Iepriekšēja ārstēšana ar vairākām 600 mg rifampicīna devām, kam seko viena 400 mg Glivec deva, samazināja Cmax un AUC (0-∞) vismaz 54% un 74% salīdzinājumā ar to vērtībām bez ārstēšanas ar rifampicīnu. Līdzīgi rezultāti tika novēroti pacientiem ar ļaundabīgu gliomu, kas ārstēti ar Glivec, vienlaikus lietojot enzīmus inducējošus pretepilepsijas līdzekļus (EIAED), piemēram, karbamazepīnu, okskarbazepīnu Imatiniba plazmas AUC samazinājās par 73%, salīdzinot ar pacientiem, kuri netika ārstēti ar EIAED. Jāizvairās no vienlaicīgas rifampicīna vai spēcīgu CYP3A4 induktoru un imatiniba lietošanas. Aktīvās vielas, kuru koncentrāciju plazmā var mainīt Glivec Imatinibs palielina simvastatīna (CYP3A4 substrāts) vidējās Cmax un AUC vērtības attiecīgi 2 un 3,5 reizes, norādot uz "imatiniba izraisītu CYP3A4 inhibīciju. Tāpēc, lietojot Glivec kopā ar CYP3A4 substrātiem ar aizvērtu terapeitisko logu, ieteicams ievērot piesardzību ( piemēram, ciklosporīns, pimozīds, takrolims, sirolims, ergotamīns, diergotamīns, fentanils, alfentanils, terfenadīns, bortezomibs, docetaksels un hinidīns). Glivec var palielināt citu CYP3A4 metabolizēto zāļu (piemēram, benzidodiazola-triazola), dažu kalcija kanālu blokatoru, koncentrāciju plazmā. HMG-CoA reduktāzes inhibitori, piemēram, statīni utt.). Sakarā ar zināmu paaugstinātu asiņošanas risku saistībā ar imatiniba lietošanu (piemēram, asiņošana), pacientiem, kuriem nepieciešami antikoagulanti, kumarīna atvasinājumu, piemēram, varfarīna, vietā jāsaņem standarta vai zemas molekulmasas heparīns. In vitro Glivec inhibē citohroma P450 izoenzīma CYP2D6 aktivitāti koncentrācijās, kas ir līdzīgas tām, kas ietekmē CYP3A4 aktivitāti. Imatinib 400 mg divas reizes dienā inhibēja metoprolola metabolismu, ko ietekmē CYP2D6, un AUC palielinājās par aptuveni 23% (90 % TI [1,16-1,30]). Šķiet, ka devas pielāgošana nav nepieciešama, ja imatinibu lieto vienlaikus ar CYP2D6 substrātiem, tomēr jāievēro piesardzība, lietojot CYP2D6 substrātus ar šauru terapeitisko logu, piemēram, metoprololu. Pacientiem, kuri tiek ārstēti ar metoprololu, jāapsver klīniskā uzraudzība. In vitroGlivec inhibē paracetamola O-glikuronidāciju ar Ki vērtību 58,5 mikromoli / l. Šī inhibīcija netika novērota in vivo pēc 400 mg Glivec un 1000 mg paracetamola ievadīšanas. Lielākas Glivec un paracetamola devas nav pētītas. Tādēļ jāievēro piesardzība, vienlaikus lietojot lielas Glivec un paracetamola devas. Pacientiem ar vairogdziedzera darbības traucējumiem, kuri saņem levotiroksīnu, vienlaikus lietojot Glivec, levotiroksīna ekspozīcija plazmā var samazināties (skatīt 4.4. Apakšpunktu).Tomēr novērotās mijiedarbības mehānisms pašlaik nav zināms. Ir klīniskā pieredze par Glivec lietošanu vienlaikus ar ķīmijterapiju pacientiem ar Ph + ALL (skatīt 5.1. Apakšpunktu), taču zāļu mijiedarbība starp imatinibu un ķīmijterapijas shēmām nav pilnībā raksturota. Var pastiprināties imatiniba blakusparādības, piemēram, hepatotoksicitāte, mielosupresija vai citas, un ir ziņots, ka vienlaicīga lietošana ar L-asparagināzi var būt saistīta ar paaugstinātu hepatotoksicitāti (skatīt apakšpunktu 4.8). Tādēļ Glivec lietošanai kombinācijā nepieciešama īpaša piesardzība. Sievietes reproduktīvā vecumā Sievietes reproduktīvā vecumā jāinformē par nepieciešamību ārstēšanas laikā lietot efektīvu kontracepcijas līdzekli. Grūtniecība Dati par imatiniba lietošanu grūtniecēm ir ierobežoti. Tomēr pētījumi ar dzīvniekiem parādīja reproduktīvo toksicitāti (skatīt 5.3. Apakšpunktu) un iespējamais risks auglim nav zināms. Glivec nedrīkst lietot grūtniecības laikā. Ja vien tas nav absolūti nepieciešams. grūtniecību, informējiet pacientu par iespējamo risku auglim. Barošanas laiks Ir ierobežota informācija par imatiniba izplatīšanos mātes pienā. Novērtējumi divām barojošām sievietēm parādīja, ka gan imatinibu, gan tā aktīvo metabolītu var izdalīt mātes pienā. Vienam pacientam novērtētā piena / plazmas attiecība bija 0,5 imatinibam un 0,9 metabolītam, kas liecina par lielāku metabolīta sadalījumu pienā. Ņemot vērā imatiniba un tā metabolīta kopējo koncentrāciju un zīdaiņu maksimālo piena dienas devu, šķiet, ka kopējā iedarbība ir zema (aptuveni 10% no terapeitiskās devas). Tomēr, tā kā zema iedarbības devu ietekme zīdaiņiem ir nav zināms, sievietes, kuras lieto imatinibu, nedrīkst barot bērnu ar krūti. Auglība Neklīniskajos pētījumos žurku tēviņu un mātīšu auglība netika ietekmēta (skatīt apakšpunktu 5.3). Nav veikti pētījumi ar Glivec ārstētiem pacientiem, lai novērtētu tā ietekmi uz auglību un spermatoģenēzi.Pacientiem, kuri Glivec terapijas laikā uztraucas par savu auglību, jākonsultējas ar savu ārstu. Pacienti jābrīdina, ka ārstēšanas laikā ar imatinibu var rasties nevēlamas blakusparādības, piemēram, reibonis, neskaidra redze vai miegainība. Tāpēc ieteicams vadīt transportlīdzekļus un apkalpot mehānismus. Pacientiem ar progresējošu vēzi var būt vairāki neskaidri klīniskie apstākļi, kas apgrūtina nevēlamo blakusparādību cēloņu novērtēšanu, ņemot vērā dažādus simptomus, kas saistīti ar pamata slimību, tās progresēšanu un vienlaicīgu daudzu medikamentu lietošanu. HML klīniskajos pētījumos zāļu izņemšana ar zālēm saistītu blakusparādību dēļ tika novērota 2,4% no nesen diagnosticētiem pacientiem, 4% pacientu progresējošā hroniskā fāzē pēc interferona terapijas neveiksmes, 4% pacientu progresējošā hroniskā fāzē. Paātrināta fāzes pacientiem pēc interferona terapijas neveiksmes un 5% pacientu ar blastu krīzi pēc interferona terapijas neveiksmes. GIST pētījumos zāļu lietošana tika pārtraukta 4% pacientu ar zālēm saistītu blakusparādību dēļ. Blakusparādības bija līdzīgas visās indikācijās, ar diviem izņēmumiem. HML pacientiem tika novērota lielāka mielosupresija nekā GIST pacientiem, kas, iespējams, ir pamatslimības dēļ. Pētījumā, kurā piedalījās pacienti ar neatgriezenisku un / vai metastātisku GIST, 7 pacientiem (5%) bija CTC 3./4. Pakāpes GI asiņošana (3 pacienti), asiņošana audzēja iekšienē (3 pacienti) vai abi (1 pacients). GI asiņošanas cēlonis varēja būt GI audzēju atrašanās vieta (skatīt apakšpunktu 4.4). GI asiņošana un audzēja asiņošana var būt nopietna un dažreiz letāla. Visbiežāk (≥10%) ar zālēm saistītās blakusparādības, par kurām ziņots abos gadījumos, bija viegla slikta dūša, vemšana, caureja, sāpes vēderā, nogurums, mialģija, muskuļu krampji un izsitumi. Visos pētījumos parasti tika konstatēta virspusēja tūska, kas galvenokārt aprakstīta kā periorbitāla vai apakšējo ekstremitāšu tūska. Tomēr šīs tūskas reti bija smagas, un tās var ārstēt ar diurētiskiem līdzekļiem, citiem atbalsta līdzekļiem vai samazinot Glivec devu. Ja imatinibu kombinēja ar lielām ķīmijterapijas devām pacientiem ar Ph + ALL, tika novērota pārejoša aknu toksicitāte paaugstināta transamināžu līmeņa un hiperbilirubinēmijas izteiksmē. Ņemot vērā ierobežoto drošības informāciju, līdz šim ziņotās blakusparādības bērniem atbilst drošības profilam, kas noteikts pieaugušiem Ph + ALL pacientiem. Drošības informācija bērniem ar Ph + ALL ir ļoti ierobežota, tomēr jaunas drošības problēmas nav atklātas. Dažādas blakusparādības, piemēram, izsvīdumu pleirā, ascītu, plaušu tūsku un strauju svara pieaugumu ar virspusēju tūsku vai bez tās, var kopīgi raksturot kā "šķidruma aizturi". Šīs reakcijas parasti var pārvaldīt, īslaicīgi pārtraucot Glivec un diurētisko līdzekļu lietošanu un citus atbilstošus atbalstošus terapeitiskus pasākumus. Tomēr dažas no šīm reakcijām var būt nopietnas vai dzīvībai bīstamas, un vairāki pacienti ar blastu krīzi ir miruši ar sarežģītu klīnisko ainu par pleiras izsvīdumu, sastrēguma sirds mazspēju un nieru mazspēju. Klīniskajos pētījumos, kas tika veikti ar pediatriskiem pacientiem, netika atklāts īpašs drošības aspekts. Nevēlamās reakcijas Blakusparādības, par kurām ziņots vairāk nekā vienā atsevišķā gadījumā, ir uzskaitītas zemāk pēc orgānu sistēmas klasēm un biežuma. Biežuma kategorijas ir definētas, izmantojot šādu iedalījumu: ļoti bieži (≥1 / 10), bieži (≥1 / 100, Katrā sastopamības biežumā nevēlamās blakusparādības ir uzskaitītas biežuma secībā, vispirms visbiežāk. 1. tabulā norādītās blakusparādības un to biežums ir balstīts uz galvenajiem galvenajiem pētījumiem. 1. tabula Blakusparādības klīniskajos pētījumos 1 Par pneimoniju visbiežāk ziņots pacientiem ar progresējošu HML un pacientiem ar GIST. 2 Galvassāpes bija biežākas GIST pacientiem. 3 Pamatojoties uz pacienta gadu, sirdsdarbības traucējumi, ieskaitot sastrēguma sirds mazspēju, biežāk tika novēroti pacientiem ar progresējošu HML nekā pacientiem ar hronisku HML. Sārtums bija biežāks pacientiem ar GIST, un asiņošana (hematoma, asiņošana) bija biežāka GIST un progresējošas HML (AP-HML un HMLBC) pacientiem. 5 Par pleiras izsvīdumu biežāk ziņots pacientiem ar GIST un pacientiem ar progresējošu HML (CML-AP un CML-BC) nekā pacientiem ar hronisku HML. 6 + 7 Sāpes vēderā un kuņģa -zarnu trakta asiņošana visbiežāk tika novērotas pacientiem ar GIST. 8 Ir ziņots par dažiem letāliem aknu mazspējas un aknu nekrozes gadījumiem. Skeleta -muskuļu sāpes un ar tām saistīti notikumi biežāk tika novēroti HML pacientiem nekā GIST pacientiem. No Glivec pēcreģistrācijas pieredzes galvenokārt ziņots par šādu veidu reakcijām. Tie ietver spontānus ziņojumus un nopietnas blakusparādības, par kurām ziņots notiekošajos pētījumos, paplašinātās piekļuves programmās, klīniskās farmakoloģijas pētījumos un izpētes pētījumos ar neapstiprinātām indikācijām. nezināmu izmēru, ne vienmēr ir iespējams ticami novērtēt to biežumu vai noteikt cēloņsakarību ar imatiniba iedarbību. 2. tabula Blakusparādības pēcreģistrācijas ziņojumos 1 Ir ziņots par letāliem gadījumiem pacientiem ar progresējošu slimību, smagām infekcijām, smagu neitropēniju un citiem nopietniem blakus apstākļiem. Anomālijas laboratorijas analīzēs: Hematoloģija HML gadījumā citopēnijas un jo īpaši neitropēnija un trombocitopēnija bija izplatīta visos pētījumos, norādot uz lielāku biežumu, lietojot lielas devas ≥750 mg (I fāzes pētījums). Tomēr tika konstatēts, ka arī citopēnijas rašanās ir skaidri atkarīga no slimības stadijas. slimība, neitropēnijas biežums (ANC Nesen diagnosticētas HML hroniskas fāzes gadījumā neitropēnija (ANC) Tomēr retos gadījumos tās var pārtraukt ārstēšanu. Pediatriskiem pacientiem ar HML visbiežāk novērotā toksicitāte bija 3. vai 4. pakāpes citopēnija, ieskaitot neitropēniju, trombocitopēniju un anēmiju. Tās parasti parādījās pirmajos terapijas mēnešos. Pētījumā ar pacientiem ar neatgriezenisku un / vai metastātisku GIST 3. un 4. pakāpes anēmija tika ziņota attiecīgi 5,4% un 0,7% pacientu, kas vismaz dažiem no šiem pacientiem varētu būt saistīta ar kuņģa-zarnu trakta vai audzēja iekšēju asiņošanu. 3. un 4. pakāpes neitropēnija tika novērota attiecīgi 7,5% un 2,7% pacientu, bet 3. pakāpes trombocitopēnija - 0,7% pacientu. Nevienam pacientam neattīstījās 4. pakāpes trombocitopēnija. Leikocīti (WBC) un neitrofilo leikocītu skaits pārsvarā parādījās pirmajās sešās nedēļās. terapiju, un pēc tam vērtības saglabājas samērā stabilas. Bioķīmija HML pacientiem tika novērota smaga 3. vai 4. pakāpes transamināžu (alanīna aminotransferāzes) līmeņa paaugstināšanās un 4.8% 3. vai 4. pakāpes aspartātaminotransferāzes (ASAT) līmeņa paaugstināšanās. Ir bijuši citolītiska un holestātiska hepatīta un aknu mazspējas gadījumi; dažos gadījumos iznākums bija letāls, tostarp viens pacients tika ārstēts ar lielām paracetamola devām. Ziņošana par iespējamām blakusparādībām Ir svarīgi ziņot par iespējamām blakusparādībām, kas radušās pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālisti tiek lūgti ziņot par visām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu. Pieredze ar devām, kas ir lielākas par ieteicamo terapeitisko devu, ir ierobežota. Atsevišķi Glivec pārdozēšanas gadījumi ir ziņoti spontāni un literatūrā. Pārdozēšanas gadījumā pacients ir jānovēro un jāveic atbilstoša simptomātiska ārstēšana. Parasti ziņots par rezultātiem šajos gadījumos gadījumi ir "uzlaboti" vai "fiksēti". Dažādos devu intervālos ziņots par šādiem notikumiem: Pieaugušo populācija 1200-1600 mg (ārstēšanas ilgums no 1 līdz 10 dienām): slikta dūša, vemšana, caureja, izsitumi, eritēma, tūska, pietūkums, nogurums, muskuļu spazmas, trombocitopēnija, pancitopēnija, sāpes vēderā, galvassāpes, samazināta ēstgriba. 1800-3200 mg (līdz 3200 mg dienā 6 dienas): vājums, mialģija, paaugstināts kreatīna fosfokināzes līmenis, paaugstināts bilirubīna līmenis, sāpes kuņģa-zarnu traktā. 6400 mg (viena deva): Literatūrā ziņots par gadījumu, kad pacientam bija slikta dūša, vemšana, sāpes vēderā, drudzis, sejas pietūkums, samazināts neitrofilu skaits, palielināts transamināžu līmenis. 8-10 g (viena deva): ziņots par vemšanu un kuņģa-zarnu trakta sāpēm. Pediatriskā populācija Vienam 3 gadus vecam bērnam, kurš tika pakļauts vienreizējai 400 mg devai, bija vemšana, caureja un anoreksija, un citam 3 gadus vecam bērnam, kas tika pakļauts vienreizējai 980 mg devai, bija samazināts balto asins šūnu skaits un caureja. Pārdozēšanas gadījumā pacients ir jānovēro un jāveic atbilstoša atbalstoša ārstēšana. Farmakoterapeitiskā grupa: proteīna tirozīnkināzes inhibitors, ATĶ kods: L01XE01 Darbības mehānisms Imatinibs ir maza proteīna-tirozīnkināzes inhibitora molekula, kas spēcīgi inhibē Bcr-Abl tirozīnkināzes, kā arī vairāku tirozīnkināzes receptoru aktivitāti: komplekts, cilmes šūnu faktora (SCF) receptors, ko kodē proto-onkogēna c-Kit , diskoidīna domēna receptorus (DDR1 un DDR2), koloniju stimulējošā faktora receptorus (CSF-1R) un alfa un beta receptorus trombocītu izcelsmes augšanas faktoram (PDGFR-alfa un PDGFR-beta). Imatinibs var arī kavēt šūnu notikumus, ko izraisa šo kināzes receptoru aktivācija. Farmakodinamiskā iedarbība Imatinibs ir proteīna-tirozīnkināzes inhibitors, kas spēcīgi inhibē Bcr-Abl tirozīnkināzi in vitro, šūnu līmenī e in vivo. Savienojums selektīvi inhibē proliferāciju un izraisa apoptozi Bcr-Abl pozitīvās šūnu līnijās un svaigās leikēmijas šūnās no Filadelfijas hromosomu pozitīvās HML un akūtas limfoblastiskās leikēmijas (ALL) pacientiem. In vivo savienojumam piemīt pretvēža aktivitāte kā atsevišķs līdzeklis dzīvnieku modeļos ar Bcr-Abl pozitīvām audzēja šūnām. Imatinibs ir arī tirozīnkināzes receptoru inhibitors trombocītu izcelsmes augšanas faktoram (PDGF), PDGF-R un cilmes šūnu faktoram (SCF), c-Kit, un kavē PDGF un SCF mediētos šūnu notikumus. In vitro, imatinibs kavē proliferāciju un izraisa apoptozi kuņģa -zarnu trakta stromas audzēja (GIST) šūnās, kas izsaka aktīvu komplekts. MDG / MPD, HES / CLE un DFSP patoģenēzē ir iesaistīta PDGF receptoru vai Abl proteīna tirozīnkināzes konstitutīva aktivizēšana dažādu partneru proteīnu saplūšanas vai konstitutīvas PDGF ražošanas rezultātā. Imatinibs kavē signalizāciju un šūnu proliferāciju. ar PDGFR ierobežojumu atcelšanu un Abl kināzes aktivitāti. Hroniskas mieloleikozes klīniskie pētījumi Glivec efektivitāte balstās uz vispārējām hematoloģiskās un citoģenētiskās atbildes vērtībām un slimības dzīvildzi bez slimības progresēšanas. Izņemot nesen diagnosticētu hroniskas fāzes HML, nav veikti nekādi kontrolēti klīniskie pētījumi, kas pierādītu klīnisko ieguvumu, kas nozīmē, ar slimību saistītie simptomi vai paaugstināta dzīvildze. Tika veikti trīs lieli, atklāti, nekontrolēti II fāzes starptautiskie pētījumi ar Filadelfijas hromosomu pozitīviem (Ph +) HML pacientiem ar progresējošu, paātrinātu vai blastu krīzes slimību. citas Ph + leikēmijas vai hroniskas fāzes HML, bet kam nebija ieguvuma no iepriekšējās alfa interferona (IFN) terapijas, tika veikts liels, randomizēts, atklāts, III fāzes starptautiskais pētījums ar pacientiem ar nesen diagnosticētu Ph + HML. Turklāt pediatriskie pacienti tika ārstēti divos I fāzes un vienā II fāzes pētījumos. Visos klīniskajos pētījumos 38-40% pacientu bija ≥60 gadus veci un 10-12% pacientu bija ≥70 gadus veci. Hroniska fāze, jauna diagnoze: Šajā III fāzes pētījumā pieaugušiem pacientiem salīdzināja ārstēšanu tikai ar Glivec un alfa interferona (IFN) un citarabīna (Ara-C) kombināciju. Pacienti, kuri nereaģēja (6 mēnešu laikā nebija pilnīgas hematoloģiskas atbildes reakcijas (REC), balto asins šūnu skaita palielināšanās (WBC)), nebija nozīmīgas citoģenētiskās atbildes reakcijas (MCR) 24 mēnešu laikā), kuriem bija atbildes reakcijas zudums ( REC un MCR) vai smaga ārstēšanas nepanesamība, tika atļauts pāriet uz alternatīvu ārstēšanu. Glivec grupā pacienti tika ārstēti ar 400 mg dienas devām. IFN grupā pacienti tika ievadīti subkutāni ar IFN devām 5 MIU / m2 / dienā kombinācijā ar Ara-C devā 20 mg / m2 / dienā 10 dienas mēnesī. Pavisam randomizēti 1106 pacienti, pa 553 katrā rokā. Abu grupu sākotnējās īpašības bija līdzīgas. Vidējais vecums bija 51 gads (diapazons no 18 līdz 70 gadiem), 21,9% pacientu vecumā no 60 gadiem. 59% bija vīrieši un 41% sievietes; 89,9% bija kaukāzieši un 4,7% melni. Septiņus gadus pēc pēdējā pacienta uzņemšanas vidējais pirmās līnijas ārstēšanas ilgums bija attiecīgi 82 un 8 mēneši Glivec grupā un IFN grupā. Vidējais otrās līnijas ārstēšanas ilgums ar Glivec bija 64 mēneši. Kopumā pacientiem, kuri pirmo reizi ārstējās ar Glivec, vidējā dienas deva bija 406 ± 76 mg. Pētījuma galvenais efektivitātes parametrs ir dzīvildze bez slimības progresēšanas. Progresēšana tika definēta kā viens no šiem: progresēšana paātrinātā fāzē vai blastu krīze, nāve, pilnīgas hematoloģiskās atbildes reakcijas (REC) vai lielas citoģenētiskās atbildes reakcijas (MCR) zudums vai pacientiem, kuri nesasniedz REC, balto asins šūnu skaita palielināšanās, neraugoties uz atbilstošu terapeitisko vadību. Galvenie sekundārie parametri ir nozīmīga citoģenētiskā reakcija, hematoloģiskā reakcija, molekulārā reakcija (atlikušais slimības novērtējuma minimums), laiks līdz paātrinātajai fāzei un blastu krīze un izdzīvošana Rezultāti ir parādīti 3. tabulā. 3. tabula Atbilde nesen diagnosticētā HML pētījumā (84 mēnešu dati) * lpp ** Molekulārās reakcijas rādītāji ir balstīti uz pieejamajiem paraugiem Hematoloģiskās atbildes kritēriji (visas atbildes jāapstiprina vismaz pēc 4 nedēļām): WBC Citoģenētiskās atbildes kritēriji: pilnīga (0%Ph + metafāžu), daļēja (1-35%), neliela (36-65%) vai minimāla (66-95%). Galvenā atbilde (0–35%) apvieno gan pilnīgas, gan daļējas atbildes. Galvenie molekulārās atbildes kritēriji: perifērās asinīs Bcr-Abl transkripta samazinājums ≥ 3 log (samazināts ar kvantitatīvo reversās transkriptāzes RT-PCR), salīdzinot ar standartizēto sākotnējo līmeni. Pilnīgas hematoloģiskās atbildes reakcijas, galvenās citoģenētiskās atbildes reakcijas un pilnīgas citoģenētiskās atbildes reakcijas ātrums pirmās rindas terapijā tika aprēķināts saskaņā ar Kaplana-Meiera metodi, saskaņā ar kuru atbildes reakcijas tika saīsinātas pēdējā novērtējuma datumā. Izmantojot šo metodi, kumulatīvā reakcija rādītāji, kas tika aprēķināti pirmās rindas ārstēšanai ar Glivec, bija labāki no 12 mēnešiem līdz 84 terapijas mēnešiem šādi: CHR attiecīgi no 96,4% līdz 98,4% un CCyR attiecīgi no 69, 5% līdz 87,2%. Pēc 7 gadu novērošanas Glivec grupā bija 93 (16,8%) progresēšanas gadījumi: 37 (6,7%) paātrinātās fāzes progresēšanas / blastu krīze, 31 (5,6%) MCyR zudums, 15 (2,7%) CHR zudums vai balto asins šūnu skaita palielināšanās un 10 gadījumi (1,8%) ar HML nesaistītas nāves gadījumi. Ārstēšanā ar IFN + Ara-C bija 165 gadījumi (29,8%), no kuriem 130 notika pirmās rindas terapijas laikā ar IFN + Ara-C. Paredzētais pacientu skaits bez progresēšanas līdz paātrinātai fāzei vai blastu krīzei 84 mēnešu laikā bija ievērojami augstāks Glivec grupā nekā IFN grupā (92,5% pret 85,1%, p Glivec un IFN + Ara-C grupās bija 71 (12,8%) un 85 (15,4%) nāves gadījumi. Kopējā dzīvildze pēc 84 mēnešiem ir 86,4% Glivec randomizācijas grupā un 83,3% attiecīgi IFN + Ara-C grupā (log-rank tests p = 0,073). "Laiku līdz notikumam" beigu punktu lielā mērā ietekmē "lielais šķērsošanas procents no IFN + Ara-C grupas līdz Glivec grupai. Glivec terapijas ietekmi uz izdzīvošanu nesen diagnosticētas hroniskas fāzes HML vēl vairāk novērtēja "iepriekš izklāstīto Glivec datu un citu III fāzes pētījuma primāro datu retrospektīva analīze, izmantojot IFN + Ara-C (n = 325) ar identisku dozēšanas režīmu. Šajā retrospektīvajā analīzē tika pierādīts Glivec pārākums pret IFN + Ara -C kopējā izdzīvošanas ziņā (lpp Citoģenētiskās un molekulārās atbildes pakāpe acīmredzami ietekmēja ilgtermiņa rezultātus pacientiem, kuri saņēma Glivec. Lai gan aptuveni 96% (93%) pacientu ar CCyR (PCyR) 12 mēnešu laikā bez progresēšanas līdz paātrinātai fāzei / blastu krīzei bija 84 mēneši, tikai 81% pacientu bez MCyR 12 mēnešu laikā bez slimības progresēšanas progresējošs posms 84 mēnešos (globālais lpp Šajā pētījumā atļautā devas palielināšana bija no 400 mg dienā līdz 600 mg dienā, pēc tam no 600 mg dienā līdz 800 mg dienā. Pēc 42 mēnešu novērošanas 11 pacientiem tika konstatēts citoģenētiskās atbildes zaudējums (vairāk nekā 4 nedēļas). No šiem 11 pacientiem 4 pacientiem deva tika palielināta līdz 800 mg dienā, 2 no tiem atjaunojoties citoģenētiskajai reakcijai (1 daļēja un 1 pilnīga, pēdējā sasniedza arī molekulāro atbildes reakciju), savukārt no 7 pacientiem, kuriem viņi nebija palielinājusi devu, tikai viens bija atguvis pilnu citoģenētisko reakciju. Dažu blakusparādību biežums bija lielāks 40 pacientiem, kuriem dienas deva tika palielināta līdz 800 mg, salīdzinot ar pacientu populāciju pirms devas palielināšanas (n = 551). Visbiežāk novērotās blakusparādības bija asiņošana no kuņģa -zarnu trakta, konjunktivīts un transamināzes vai bilirubīns Ir ziņots par citām blakusparādībām ar tādu pašu vai mazāku biežumu. Hroniska fāze, interferona terapijas neveiksme: 532 pieaugušie pacienti tika ārstēti ar sākuma devu 400 mg. Pacienti tika iedalīti trīs galvenajās kategorijās: hematoloģiska nepietiekamība (29%), citoģenētiska nepietiekamība (35%) vai interferona nepanesamība (36%).Pacienti iepriekš bija saņēmuši vidēji 14 mēnešus ilgu IFN terapiju devās ≥25 x 106 SV nedēļā, un visi bija hroniskā progresējošā fāzē, un vidējais laiks no diagnozes bija 32 mēneši. Pētījuma primārais efektivitātes mainīgais lielākais bija citoģenētiskās atbildes reakcijas ātrums (pilnīga plus daļēja atbildes reakcija, 0 līdz 35% Ph + metafāžu kaulu smadzenēs). Šajā pētījumā 65% pacientu sasniedza nozīmīgu citoģenētisku reakciju, kas bija pilnīga 53% pacientu (apstiprināts 43%) (4. tabula). Pilnīga hematoloģiska reakcija tika sasniegta 95% pacientu. Paātrināta fāzePētījumā tika iekļauti 235 pieaugušie pacienti ar paātrinātas fāzes slimību. Pirmie 77 pacienti sāka ārstēšanu ar 400 mg, vēlāk protokols tika pielāgots, lai varētu lietot lielākas devas, un pārējie 158 pacienti sāka ārstēšanu ar 600 mg. Primārais efektivitātes mainīgais bija hematoloģiskās atbildes reakcijas ātrums, ziņots par pilnīgu hematoloģisku atbildes reakciju, bez leikēmijas pazīmēm (t.i., blastu attīrīšana no smadzenēm un asinīm, bet bez pilnīgas perifēro asiņu atjaunošanās, kā tas ir pilnīgas atbildes gadījumā). Vai atgriešanās HML hroniskā fāzē . Apstiprināta hematoloģiskā atbildes reakcija tika sasniegta 71,5% pacientu (4. tabula). Svarīgi, ka atbilstoša citoģenētiskā reakcija tika sasniegta arī 27,7% pacientu, kas bija pilnīga 20,4% pacientu (apstiprināts 16%). Pacientiem, kuri tika ārstēti ar 600 mg, pašreizējā vidējā dzīvildze bez progresēšanas un kopējā dzīvildze bija attiecīgi 22,9 un 42,5 mēneši. Mieloīdā sprādziena krīze: Tika iekļauti 260 pacienti ar mieloīdo blastu krīzi. 95 (37%) pacienti iepriekš bija saņēmuši ķīmijterapiju paātrinātas fāzes slimības vai blastu krīzes ārstēšanai ("iepriekš ārstēti pacienti"), bet 165 (63%) nebija ārstēti ("neārstēti pacienti"). Pirmie 37 pacienti sāka ārstēšanu ar 400 mg, vēlāk protokols tika koriģēts, lai atļautu lielākas devas, un atlikušie 223 pacienti sāka ārstēšanu ar 600 mg. Primārais efektivitātes mainīgais bija hematoloģiskās atbildes reakcijas ātrums, kas tika ziņots par pilnīgu hematoloģisku reakciju, bez leikēmijas pazīmēm vai HML hroniskas fāzes atgriešanās, izmantojot tos pašus kritērijus kā paātrinātās fāzes pētījumā. Šajā pētījumā 31% pacientu sasniedza hematoloģisku atbildes reakciju (36% iepriekš neārstētiem pacientiem un 22% iepriekš ārstētiem pacientiem). Tādēļ atbildes reakcija bija augstāka pacientiem, kuri tika ārstēti ar 600 mg (33%), nekā pacientiem, kuri tika ārstēti ar 400 mg (16%, p = 0,0220). Iepriekš neārstētu un ārstētu pacientu vidējais izdzīvošanas novērtējums bija attiecīgi 7,7 un 4,7 mēneši. Limfoīdo sprādzienu krīzeI fāzes pētījumos tika iekļauts ierobežots pacientu skaits (n = 10). Hematoloģiskās atbildes reakcija bija 70%, ilgums bija 2–3 mēneši. 4. tabula. Reakcija pieaugušo HML pētījumos Pediatriskie pacienti: Kopumā 26 vecuma pediatrijas pacienti Pacienti tika ārstēti ar Glivec devām 260 mg / m2 dienā (n = 5), 340 mg / m2 dienā (n = 9), 440 mg / m2 dienā (n = 7) un 570 mg / m2 dienā. mirst (n = 5). Starp 9 pacientiem ar HML hroniskā fāzē, par kuriem bija pieejami citoģenētiskie dati, attiecīgi 4 (44%) un 3 (33%) sasniedza pilnīgu un daļēju citoģenētisko reakciju, lai iegūtu augstāku citoģenētiskās atbildes reakciju (MCR) nekā 77%. Pavisam 51 pediatrisks pacients ar nesen diagnosticētu, neārstētu hroniskas fāzes HML tika iekļauts atklātā, vienas rokas, daudzcentru, II fāzes pētījumā. Pacienti tika ārstēti ar Glivec 340 mg / m2 / dienā bez pārtraukumiem, ja nebija devu ierobežojošas toksicitātes. Pediatriskiem pacientiem ar nesen diagnosticētu HML ārstēšana ar Glivec izraisīja ātru atbildes reakciju ar pilnīgu hematoloģisko atbildes reakciju (REC) 78% pēc 8 terapijas nedēļām. Augsts REC līmenis bija saistīts ar pilnīgas citoģenētiskās atbildes reakcijas (CCyR) attīstību 65% apmērā, kas ir salīdzināma ar pieaugušajiem novērotajiem rezultātiem. Turklāt 16% gadījumu atbildes reakcijai tika novērota daļēja citoģenētiskā reakcija (PCyR). lielāks (MCyR) nekā 81%. Lielākajai daļai pacientu, kuri sasniedza pilnīgu citoģenētisko atbildes reakciju (CCyR), CCyR parādījās no 3. līdz 10. mēnesim, un vidējais laiks līdz atbildes reakcijai, pamatojoties uz Kaplana-Meiera novērtējumu, bija 5,6 mēneši. Eiropas Zāļu aģentūra ir atbrīvojusi no pienākuma iesniegt pētījumu rezultātus ar Glivec visās pediatriskās populācijas apakšgrupās ar Filadelfijas hromosomu pozitīvu hronisku mieloleikozi (bcr-abl translokācija) (informāciju par lietošanu bērniem skatīt 4.2. Apakšpunktā). Klīniskie pētījumi Ph + ALL Nesen diagnosticēts Ph + ALL: Kontrolētā pētījumā (ADE10) par imatinibu salīdzinājumā ar indukcijas ķīmijterapiju 55 nesen diagnosticētiem 55 gadus veciem un vecākiem pacientiem imatinibs, ko lietoja kā vienu līdzekli, izraisīja ievērojami lielāku pilnīgu hematoloģisko reakciju biežumu nekā ķīmijterapija (96,3% pret 50%; p = Kad glābšanas terapija ar imatinibu tika sniegta pacientiem, kuri nereaģēja vai nepietiekami reaģēja uz ķīmijterapiju, tika novērots, ka 9 pacienti (81,8%) no 11 bija sasnieguši pilnīgu hematoloģisku atbildes reakciju. Šī klīniskā iedarbība bija saistīta ar lielāku bcr- abl transkriptu pacientiem, kuri tika ārstēti ar imatinibu, nekā pacientiem, kuri tika ārstēti ar ķīmijterapiju pēc 2 terapijas nedēļām (p = 0,02). Visi pacienti bija saņēmuši imatiniba un konsolidācijas ķīmijterapiju (skatīt 5. tabulu) pēc indukcijas fāzes un bcr-abl transkripta līmeņiem nedēļā 8 bija identiski abās rokās. Kā tika prognozēts pētījuma plānā, netika novērota atšķirība remisijas ilgumā, izdzīvošanā bez slimībām vai kopējā dzīvildzē, lai gan pacientiem ar pilnīgu molekulāro atbildes reakciju un kuriem bija minimāla atlikušā slimība, bija labāks iznākums abu ilgumu ziņā. p = 0,01) un dzīvildze bez slimībām (p = 0,02). Rezultāti, kas novēroti 211 nesen diagnosticētu Ph + ALL pacientu populācijā četros nekontrolētos klīniskos pētījumos (AAU02, ADE04, AJP01 un AUS01) atbilst iepriekš aprakstītajiem rezultātiem. Imatinibs kombinācijā ar indukcijas ķīmijterapiju (skatīt 5. tabulu) sasniedza pilnīgu hematoloģiskās atbildes reakcijas rādītāju 93% (147 no 158 novērtējamiem pacientiem) un citoģenētiskās atbildes reakcijas ātrumu, kas lielāks par 90% (19 no 21 novērtējama pacienta). bija 48% (49 no 102 vērtējamiem pacientiem). Divos pētījumos (AJP01 un AUS01) dzīvildze bez slimībām (DFS) un kopējā dzīvildze (OS) konsekventi pārsniedza 1 gadu un bija labāka par vēsturisko kontroli (p DFS) 5. tabula Ķīmijterapijas shēmas, ko lieto kombinācijā ar Glivec Pediatriskie pacientiKopā 93 pediatrijas, pusaudžu un jauniešu pieaugušie ar Ph + ALL (vecumā no 1 līdz 22 gadiem) tika iekļauti III fāzes I2301, daudzcentru, atklātā, nejaušinātā, secīgā kohortas pētījumā un tika ārstēti ar Glivec ( 340 mg / m2 / dienā) kombinācijā ar intensīvu ķīmijterapiju pēc indukcijas terapijas. Glivec tika ievadīts ar pārtraukumiem 1. – 5. Kohortā, palielinoties Glivec lietošanas ilgumam un ātrāk sākoties no kohortas uz kohortu; 1. grupa saņēma zemāko Glivec devas intensitāti un 5. grupa saņēma vislielāko devas intensitāti (garākais ārstēšanas ilgums Glivec terapijas dienās, ko nepārtraukti lieto katru dienu pirmo ķīmijterapijas kursu laikā). Pacientiem 5. grupā (n = 50) Glivec nepārtraukta ikdienas iedarbība ārstēšanas kursa sākumā kombinācijā ar ķīmijterapiju uzlaboja izdzīvošanu bez notikumiem (EFS) 4 gadus, salīdzinot ar vēsturisko kontroli (n = 120), kuri bija saņēmuši standarta ķīmijterapiju bez Glivec (attiecīgi 69,6% pret 31,6%). Aprēķinātā 4 gadu OS 5. grupā bija 83,6%, salīdzinot ar 44,8% vēsturiskajā kontrolē. 20 no 50 pacientiem (40%) 5. grupā saņēma asinsrades cilmes šūnu transplantāciju. 6. tabula Ķīmijterapijas shēmas, ko lietoja kombinācijā ar Glivec pētījumā I2301 G-CSF = granulocītu augšanas faktors, VP-16 = etopozīds, MTX = metotreksāts, IV = intravenoza, SC = subkutāna, IT = intratekāla, PO = perorāla, IM = intramuskulāra, ARA-C = citarabīns, CPM = ciklofosfamīds, VCR = vinkristīns, DEX = deksametazons, DAUN = daunorubicīns, 6-MP = 6-merkaptopurīns, E.Coli L-ASP = L-asparagināze, PEG-ASP = pegilēta asparagināze, MESNA = nātrija-2-merkaptoetāna sulfonāts, iii = vai vairāk, kad MTX līmenis ir Pētījums AIT07 bija II / III fāzes daudzcentru atklāts randomizēts pētījums, kurā piedalījās 128 pacienti (no 1 līdz Ph + recidivējošs / ugunsizturīgs VISS: Lietojot imatinibu kā atsevišķu līdzekli pacientiem ar recidivējošu / refraktāru Ph + ALL, 53 pacientiem bija 30% (9% pilnīga) hematoloģiskās atbildes reakcija un 23% augstāks citoģenētiskās atbildes rādītājs no 411, ko varēja novērtēt pēc atbildes. (Precīzāk, no 411 pacientiem 353 tika ārstēti "paplašinātas piekļuves programmas kontekstā, kas neparedzēja datu vākšanu par primāro atbildes reakciju."). vidējais laiks līdz progresēšanai bija no 2,6 līdz 3,1 mēnesim, un 401 novērtējamajā pacientā vidējā kopējā dzīvildze bija no 4,9 līdz 9 mēnešiem. Dati bija līdzīgi, atkārtoti pārbaudot, iekļaujot tikai pacientus vecumā no 55 gadiem. MDS / MPD klīniskie pētījumi Pieredze par Glivec lietošanu šajā indikācijā ir ļoti ierobežota, un tā balstās uz hematoloģiskās un citoģenētiskās atbildes reakcijas rādītājiem Nav veikti kontrolēti klīniskie pētījumi, kas pierādītu klīnisko ieguvumu vai palielinātu dzīvildzi. Tika veikts atklāts daudzcentru II fāzes klīniskais pētījums (pētījums B2225), lai novērtētu Glivec dažādās pacientu grupās ar riska slimībām, kas saistītas ar Abl, Kit vai PDGFR proteīna tirozīnkināzi. Šajā pētījumā tika iekļauti 7 pacienti. Ar MDS / MPD, kas tika ārstēts ar Glivec 400 mg dienā. Trīs pacientiem bija pilnīga hematoloģiskā atbildes reakcija (CHR) un vienam pacientam bija daļēja hematoloģiska atbildes reakcija (PHR). Sākotnējās analīzes laikā trīs no četriem pacientiem ar no PDGFR gēnu pārkārtošanās viņiem bija attīstījusies hematoloģiska reakcija (2 CHR un 1 PHR). Šo pacientu vecums bija no 20 līdz 72 gadiem. Turklāt 13 publikācijās tika ziņots par vēl 24 pacientiem ar MDS / MPD. 21 pacients tika ārstēts ar Glivec 400 mg dienā, bet pārējie 3 pacienti saņēma mazākas devas. tika konstatēts vienpadsmit pacientu PDGFR gēnu pārkārtošanās, no kuriem 9 bija sasnieguši CHR un 1 PHR.Šo pacientu vecums bija no 2 līdz 79 gadiem. Nesenā publikācijā atjaunināta informācija par 6 no šiem 11 pacientiem atklāja, ka visiem pacientiem saglabājās citoģenētiskā remisija (diapazons 32-38 mēneši). Tā pati publikācija ziņoja par ilgtermiņa novērošanas datiem no 12 pacientiem (ieskaitot 5 pacientus no pētījuma B2225) ar MDS / MPD ar PDGFR gēnu pārkārtošanos. Šie pacienti bija saņēmuši Glivec vidēji 47 mēnešus (diapazons no 24 dienām līdz 60 mēnešiem). 6 no šiem pacientiem novērošana tagad pārsniedz 4 gadus. Vienpadsmit pacienti ātri sasniedza CHR, desmit no tiem pilnībā izzuda citoģenētiskās novirzes un samazinājās vai pazuda saplūšanas transkripti, kas izmērīti ar RT-PCR. Hematoloģiskā un citoģenētiskā atbildes reakcija tika saglabāta vidēji vidēji 49 mēnešus (diapazons 19–60) un 47 mēnešus (diapazons 16–59). Kopējā dzīvildze ir 65 mēneši pēc diagnozes noteikšanas (diapazons 25-234). Glivec ievadīšana pacientiem bez ģenētiskas translokācijas parasti nerada uzlabojumus. Nav kontrolētu pētījumu par pediatriskiem pacientiem ar MDS / MPD. Četrās publikācijās ir ziņots par pieciem pacientiem ar MDS / MPD, kas saistīti ar PDGFR gēnu pārkārtošanos. Šo pacientu vecums svārstījās no 3 mēnešiem līdz 4 gadiem, un imatinibu lietoja 50 mg dienā vai devās no 92,5 līdz 340 mg / m2 dienā. Visi pacienti bija sasnieguši pilnīgu hematoloģisku reakciju, citoģenētisku atbildes reakciju un / vai klīniska reakcija. HES / CLE klīniskie pētījumi Tika veikts atklāts daudzcentru II fāzes klīniskais pētījums (pētījums B2225), lai novērtētu Glivec dažādās pacientu grupās ar smagu slimību, kas saistīta ar Abl, Kit vai PDGFR proteīna tirozīnkināzēm. Šajā pētījumā 14 pacienti ar HES / CEL tika ārstēti ar Glivec dienas devas no 100 mg līdz 1000 mg. Papildu 162 pacienti ar HES / CEL, par kuriem ziņots 35 gadījumu ziņojumos un publicētās gadījumu sērijas, saņēma Glivec dienas devās no 75 mg līdz 800 mg. Tās bija citoģenētiskas novirzes, kas tika novērtētas 117 pacientiem no kopējā 176 pacientu populācijas. 61 no šiem 117 pacientiem tika identificēta kodolsintēzes kināze FIP1L1 -PDGFRα. Citos 3 publicētos dokumentos vēl četri pacienti ar HES bija pozitīvi pret FIP1L1 saplūšanas kināzi -PDGFRα. Visi 65 pacienti, pozitīvi FIP1L1-PDGFRα saplūšanas kināze bija sasniegusi CHR, kas saglabājās vairākus mēnešus (ziņošanas laikā saīsināts diapazons no 1+ līdz 44+ mēnešiem). un ziņots nesenajā publikācijā, 21 no šiem 65 pacientiem arī bija sasniedzis pilnīgu molekulāro remisiju, vidēji novērojot 28 mēnešus (diapazons 13–67 mēneši). Šo pacientu vecums bija no 25 līdz 72. Turklāt pētnieki ziņoja par klīniskiem simptomu uzlabošanās un citu funkcionālu orgānu patoloģiju gadījumiem. Ir ziņots par sirds, nervu sistēmas, ādas / zemādas audu, elpošanas / krūšu kurvja / videnes trakta, muskuļu un skeleta / saistaudu / asinsvadu un kuņģa -zarnu trakta uzlabošanos. Nav kontrolētu pētījumu par pediatriskiem pacientiem ar HES / CEL. Trīs publikācijas ziņoja par trim pacientiem ar HES un CLE, kas saistīti ar PDGFR gēnu pārkārtošanos. Šo pacientu vecums bija no 2 līdz 16 gadiem, un imatinibu lietoja devā 300 mg / m2 dienā vai 200 līdz 400 mg dienā. Visi pacienti bija sasnieguši hematoloģisku atbildes reakciju, pilnīgu citoģenētisko reakciju un / vai pilnīga molekulāra reakcija. Neoperējama un / vai metastātiska GIST klīniskie pētījumi Starptautisks, randomizēts, nekontrolēts, II fāzes atklāts pētījums tika veikts pacientiem ar neatgriezeniskiem vai metastātiskiem ļaundabīgiem kuņģa-zarnu trakta stromas audzējiem (GIST). Šajā pētījumā tika iekļauti un randomizēti 147 pacienti. Saņēma iekšķīgi 400 mg vai 600 mg vienu reizi dienā līdz 36 mēnešiem. Šie pacienti bija vecumā no 18 līdz 83 gadiem, un viņiem tika konstatēta neatgriezeniska un / vai metastātiska ļaundabīga GIST patoloģiska diagnoze. komplekts. Imūnhistoķīmiskie testi periodiski tika veikti ar Kit antivielu (A-4502, poliklonēta truša antiserums, 1: 100; DAKO Corporation, Carpinteria, CA) saskaņā ar analīzi ar avidīna-biotīna-peroksidāzes kompleksa metodi pēc antigēna atgūšanas. Primārie pierādījumi par efektivitāti bija balstīti uz objektīvām atbildes vērtībām. Audzējiem bija jābūt izmērāmiem vismaz vienā slimības punktā, un atbildes raksturojums tika balstīts uz Dienvidrietumu onkoloģijas grupas (SWOG) kritērijiem. Rezultāti ir sniegti 7. tabulā. 7. tabula Labākā audzēja reakcija pētījumā STIB2222 (GIST) Starp abām ārstēšanas grupām atbildes reakcijas atšķirības nebija. Ievērojams skaits pacientu, kuriem starpposma analīzes laikā slimība stabilizējās, ar ilgāku ārstēšanu sasniedza daļēju atbildes reakciju (vidējais novērošanas periods bija 31 mēnesis). Vidējais laiks līdz atbildes reakcijai bija 13 nedēļas (95% TI 12–23). laiks līdz ārstēšanas neveiksmei pacientiem ar atbildes reakciju bija 122 nedēļas (95% TI 106–147), bet kopējā pētījuma populācijā-84 nedēļas (95% TI 71–109). Kopējā dzīvildze nebija sasniegta. pēc 36 mēnešu novērošanas ir 68%. Divos klīniskajos pētījumos (pētījums B2222 un starpgrupu pētījums S0033) Glivec dienas deva tika palielināta līdz 800 mg pacientiem, pārejot uz mazāku dienas devu - 400 mg vai 600 mg. Kopā 103 pacientiem dienas deva tika palielināta līdz 800 mg; 6 pacienti pēc devas palielināšanas sasniedza daļēju atbildes reakciju un 21 slimības stabilizāciju, lai kopumā sasniegtu 26%klīnisko ieguvumu. No pieejamiem drošības datiem šķiet, ka dienas devas palielināšana neietekmē Glivec drošības profilu. Līdz 800 mg pacientiem pārejot uz mazāku dienas devu - 400 mg vai 600 mg. Klīniskie pētījumi par GIST adjuvantu ārstēšanu Adjuvanta ārstēšana ar Glivec tika novērtēta daudzcentru, dubultmaskētā, ilgstošā, placebo kontrolētā III fāzes pētījumā (Z9001), kurā piedalījās 773 pacienti. Šo pacientu vecums svārstījās no 18 līdz 91 gadam. Pētījumā iekļautajiem pacientiem ar imūnhistoķīmijas palīdzību tika diagnosticēta primārā GIST ar Kit proteīna ekspresiju un audzēja diametrs lielāks par 3 cm, ar pilnīgu primārās rezekcijas histoloģisku diagnozi. GIST. 14-70 dienu laikā pirms uzņemšanas. Pēc primārās GIST rezekcijas pacienti tika randomizēti vienā no divām ārstēšanas grupām: Glivec 400 mg dienā vai placebo vienu gadu. Pētījuma primārais efektivitātes beigu punkts bija dzīvildze bez recidīviem (RFS), kas definēta kā laiks no randomizācijas datuma līdz recidīva vai nāves datumam jebkura iemesla dēļ. Glivec ievērojami pagarināja RFS, 75% pacientu pēc 38 mēnešiem Glivec grupā recidīvs bija brīvs, salīdzinot ar 20 mēnešiem placebo grupā (attiecīgi 95% TI [30 - nevar novērtēt]; [14 - nevar novērtēt)]); (riska attiecība = 0,398 [0,259-0,610], lpp Atkārtošanās risks pacientiem pēc primārās GIST rezekcijas tika retrospektīvi novērtēts, pamatojoties uz šādiem prognostiskiem faktoriem: audzēja lielums, mitotiskais indekss, audzēja atrašanās vieta. Pieejami mitotiskā indeksa dati par 556 no 713 pacientiem [pacientu ar nodomu ārstēt (ITT)]. Apakšgrupu analīžu rezultāti saskaņā ar ASV Nacionālo veselības institūtu (NIH) riska klasifikāciju un Bruņoto spēku patoloģijas institūtu (AFIP) Nav parādīts ieguvums zema un ļoti zema riska grupās. Kopējais izdzīvošanas ieguvums netika novērots. 8. tabula Z9001 pētījuma kopsavilkums RFS analīzes saskaņā ar NIH un AFIP riska klasifikāciju * pilns novērošanas periods; NS - nav novērtējams Otrajā III fāzes atklātā daudzcentru pētījumā (SSG XVIII / AIO) salīdzināja 12 mēnešu ārstēšanu ar Glivec 400 mg dienā, salīdzinot ar 36 mēnešu ārstēšanu pacientiem pēc GIST ķirurģiskas rezekcijas un ar vienu no šiem faktoriem: > 5 cm un mitotiskais skaits> 5/50 lieljaudas lauki (HPF); o audzēja diametrs> 10 cm un jebkurš mitotisks skaits vai jebkura izmēra audzējs ar mitotisku skaitu> 10/50 HPF vai audzēja plīsums vēderplēves dobumā.Kopumā pētījumā piekrita un tika randomizēti 397 pacienti (199 pacienti 12 mēnešu grupā un 198 pacienti 36 mēnešu grupā), vidējais vecums bija 61 gads (diapazons 22–84 gadi). -līdz 54 mēnešiem (no nejaušināšanas datuma līdz datu pārtraukšanas datumam), kopā 83 mēneši starp pirmo randomizēto pacientu un beigu datumu. Pētījuma primārais mērķa kritērijs bija dzīvildze bez atkārtošanās (RFS), kas definēta kā laiks no randomizācijas datuma līdz recidīva vai nāves datumam jebkura iemesla dēļ. Ārstēšana ar Glivec trīsdesmit sešus mēnešus ievērojami pagarināja RFS, salīdzinot ar ārstēšanu ar Glivec 12 mēnešus (ar kopējo riska pakāpi (HR) = 0,46 [0,32; 0,65], p Turklāt ārstēšana ar Glivec trīsdesmit sešus mēnešus ievērojami pagarināja kopējo dzīvildzi (OS), salīdzinot ar ārstēšanu ar Glivec 12 mēnešus (HR = 0,45 [0,22; 0,89], p = 0,0187) (9. tabula). Ilgāks ārstēšanas ilgums (> 36 mēneši) var aizkavēt turpmāku recidīvu parādīšanos; tomēr šo pierādījumu ietekme uz kopējo dzīvildzi joprojām nav zināma. Kopējais nāves gadījumu skaits bija 25 12 mēnešu ārstēšanas grupā un 12 36 mēnešu ārstēšanas grupā. ITT analīzē, ti, iekļaujot visu pētāmo populāciju, ārstēšana ar imatinibu 36 mēnešus bija labāka par ārstēšanu 12 mēnešus. Plānotajā apakšgrupu analīzē pēc mutācijas veida pacientiem ar 11. eksonu saistītu mutāciju, HRS RF 36 ārstēšanas mēnešus bija 0,35 [95% TI: 0,22; 0,56] .Nevar izdarīt secinājumus par citām retāk sastopamām mutāciju apakšgrupām, jo novēroto notikumu skaits ir zems. 9. tabula Ārstēšana ar Glivec 12 mēnešus un 36 mēnešus (pētījums SSGXVIII / AIO) Nav veikti kontrolēti pētījumi ar pediatriskiem pacientiem ar c-Kit pozitīviem GIST. Septiņpadsmit pacienti ar GIST (ar vai bez Kit un PDGFR mutācijām) ir ziņoti 7 publikācijās. Šo pacientu vecums svārstījās no 8 līdz 18 gadiem, un imatinibs tika ievadīts gan adjuvantā, gan metastātiskā formā, lietojot dienas devas no 300 līdz 800 mg. Lielākajai daļai pediatrijas pacientu, kuri tika ārstēti ar GIST, trūka apstiprinošu datu par c-kit vai PDGFR mutācijām, kas varēja izraisīt pretrunīgus klīniskos rezultātus. Klīniskie pētījumi DFSP Tika veikts atklāts daudzcentru II fāzes klīniskais pētījums (pētījums B2225), kurā piedalījās 12 pacienti ar DFSP, kuri tika ārstēti ar Glivec 800 mg dienā.Pacientu vecums ar DFSP bija no 23 līdz 75 gadiem; DFSP bija metastātisks, ar lokālu recidīvu pēc sākotnējās ķirurģiskās rezekcijas un tika uzskatīts, ka pēc ievadīšanas pētījumā tā vairs nav noņemama. No 12 reģistrētajiem pacientiem 9 bija atbildes reakcija, no kurām viena bija pilnīga un 8 bija daļēja. Trīs no daļējas atbildes reakcijas pacientiem pēc operācijas tika atbrīvoti no slimības. Vidējais terapijas ilgums pētījumā B2225 bija 6,2 mēneši, maksimālais - 24,3 mēneši. Vēl 5 pacienti ar DFSP, kuri tika ārstēti ar Glivec, tika ziņoti 5 publicētos klīniskos gadījumos, viņu vecums bija no 18 mēnešiem līdz 49 gadiem. Publicētajā literatūrā aprakstītie pieaugušie pacienti tika ārstēti ar Glivec 400 mg (4 gadījumi) vai 800 mg dienā (1 gadījums). Pieciem pacientiem bija atbildes reakcija, no kuriem 3 bija pilnīgi un 2 bija daļēji. Terapijas vidējais ilgums publicētajā literatūrā bija no 4 nedēļām līdz vairāk nekā 20 mēnešiem. Translokācija t (17:22) [(q22: q13)] vai tās gēna produkts bija klāt gandrīz visiem pacientiem, kuri reaģēja uz Glivec terapiju. Nav kontrolētu pētījumu par pediatriskiem pacientiem ar DFSP. 3 publikācijās tika ziņots par pieciem pacientiem ar DFSP un PDGFR gēnu pārkārtošanos. Šo pacientu vecums bija no jaundzimušajiem līdz 14 gadiem, un imatinibu lietoja 50 mg dienā vai devās no 400 līdz 520 mg / m2 dienā.Visi pacienti sasniedza daļēju un / vai pilnīgu atbildes reakciju. Glivec farmakokinētika Glivec farmakokinētika tika novērtēta devu diapazonā no 25 līdz 1000 mg. Plazmas farmakokinētiskie profili tika analizēti 1. un 7. vai 28. dienā, līdz tam laikam koncentrācija plazmā bija sasniegusi līdzsvara stāvokli. Uzsūkšanās Kapsulas formas vidējā absolūtā biopieejamība ir 98%. Pēc perorālas devas imatiniba plazmas AUC līmenis pacientiem ir ļoti atšķirīgs. Lietojot kopā ar treknu maltīti, imatiniba uzsūkšanās ātrums bija minimāli samazināts (Cmax samazināšanās par 11% un Tmax pagarināšanās par 1,5 stundām). neliels AUC samazinājums (7,4%), salīdzinot ar badošanās apstākļiem. Iepriekšējās operācijas ietekme uz zāļu uzsūkšanos nav pētīta. Izplatīšana Klīniski nozīmīgās imatiniba koncentrācijās saistās ar plazmas olbaltumvielām, pamatojoties uz eksperimentiem in vitro, bija aptuveni 95%, galvenokārt ar albumīnu un alfa-skābes glikoproteīniem, minimāli saistoties ar lipoproteīniem. Biotransformācija Galvenais cirkulējošais metabolīts cilvēkiem ir piperazīna N-demetilēts atvasinājums, kuram in vitro ir līdzīga aktivitāte kā molekulai, no kuras tā iegūta. Tika konstatēts, ka šī metabolīta AUC plazmā ir tikai 16% no imatiniba AUC. Imatinibs un N-desmetil metabolīts kopā veidoja aptuveni 65% no cirkulējošās radioaktivitātes (AUC (0-48h)). Pārējā cirkulējošā radioaktivitāte bija saistīta ar vairākiem nelieliem metabolītiem. Rezultāti in vitro parādīja, ka CYP3A4 bija galvenais cilvēka P450 enzīms, kas katalizē imatiniba biotransformāciju. No visas potenciālo komedikāciju grupas (paracetamols, aciklovirs, allopurinols, amfotericīns, citarabīns, eritromicīns, flukonazols, hidroksiurīnviela, norfloksacīns, penicilīns V) tikai eritromicīns (IC50 50 mcM) un flukonazols (IC50 118 mcM inhibīcijas inhibīcija) varētu būt klīniski nozīmīga. Imatinibs in vitro izrādījās konkurējošs CYP2C9, CYP2D6 un CYP3A4 / 5 marķētu substrātu inhibitors. Ki vērtības cilvēka aknu mikrosomās bija attiecīgi 27, 7,5 un 7,9 μmol / l. Maksimālā imatiniba koncentrācija plazmā pacientiem ir 2–4 μmol / l, un tādēļ ir iespējama CYP2D6 un / vai CYP3A4 / 5 mediēta metabolisko inhibīcija vienlaicīgi lietotajām zālēm. Imatinibs neiejaucās 5-fluoruracila biotransformācijā, bet kavēja. paklitaksela metabolismu, ko izraisa CYP2C8 konkurējoša inhibīcija (Ki = 34,7 mcM). Šī Ki vērtība ir daudz augstāka nekā pacientiem paredzamais imatiniba līmenis plazmā, un tāpēc nav sagaidāma mijiedarbība, vienlaikus lietojot 5-fluoruracilu vai paklitakselu un imatinibu. Eliminācija Pamatojoties uz savienojuma (-u) atveseļošanos pēc perorālas 14C iezīmēta imatiniba devas, aptuveni 81% no devas tika konstatēts 7 dienu laikā izkārnījumos (68% devas) un urīnā (13% devas). deva sastāvēja no nemainīga imatiniba (5% urīna, 20% izkārnījumu), pārējā daļa bija metabolīti. Plazmas farmakokinētika Pēc iekšķīgas lietošanas veseliem brīvprātīgajiem t½ bija aptuveni 18 stundas, kas liecina, ka deva ir piemērota reizi dienā. Vidējais AUC pieaugums pēc devas palielināšanas bija lineārs un proporcionāls devai 25–1000 mg imatiniba diapazonā pēc iekšķīgas lietošanas, uzkrāšanās bija 1,5–2,5 reizes lielāka nekā līdzsvara stāvoklī pēc vienreizējas lietošanas. Farmakokinētika pacientiem ar GIST GIST pacientiem līdzsvara stāvokļa ekspozīcija bija 1,5 reizes lielāka nekā HML pacientiem, kuri lietoja to pašu devu (400 mg dienā). Pamatojoties uz sākotnējām populācijas farmakokinētikas analīzēm GIST pacientiem, bija trīs mainīgie (albumīns, WBC un bilirubīns) kam bija statistiski nozīmīga korelācija ar imatiniba farmakokinētiku. Albumīna vērtību samazināšanās izraisīja klīrensa samazināšanos (CL / f) un augstāku leikocītu līmeni. izraisīja CL / f samazināšanos. Tomēr šīs korelācijas Šajā pacientu populācijā aknu metastāžu klātbūtne var izraisīt aknu mazspēju un vielmaiņas traucējumus. Populācijas farmakokinētika Populācijas farmakokinētikas analīze HML pacientiem atklāja ierobežotu vecuma ietekmi uz izplatīšanās tilpumu (par 12% vairāk nekā 65 gadus veciem pacientiem). Šī atšķirība netiek uzskatīta par klīniski nozīmīgu. Ķermeņa svara ietekme uz imatiniba klīrensu ir tāda, ka 50 kg smagam pacientam paredzamais vidējais klīrenss ir 8,5 l / h, bet 100 kg smagam pacientam klīrenss palielināsies līdz 11,8 l / h. Šīs variācijas netiek uzskatītas par pietiekamām, lai varētu pielāgot devu, pamatojoties uz ķermeņa svara kilogramiem. Dzimums neietekmē imatiniba kinētiku. Farmakokinētika bērniem Tāpat kā pieaugušiem pacientiem, pēc perorālas lietošanas gan I, gan II fāzes pētījumos imatinibs ātri uzsūcas bērniem. Bērniem ievadot 260 un 340 mg / m2 dienas devu, tika sasniegta līdzīga iedarbība kā pieaugušajiem, kuri tika ārstēti ar attiecīgi 400 mg un 600 mg devām. Salīdzinot AUC (0–24) ar 8. un 1. dienas līmeni, lietojot devu 340 mg / m2 dienā, tika konstatēts, ka zāles uzkrājas 1,7 reizes vairāk nekā pēc atkārtotas vienas devas lietošanas. Pamatojoties uz kombinētu populācijas farmakokinētikas analīzi pediatriskiem pacientiem ar hematoloģiskiem traucējumiem (HML, Ph + ALL vai citiem ar imatinibu ārstētiem hematoloģiskiem traucējumiem), imatiniba klīrenss palielinās, palielinoties ķermeņa virsmas laukumam (BSA). Pēc BSA ietekmes korekcijas citi demogrāfiskie faktori, piemēram, vecums, ķermeņa svars un ķermeņa masas indekss, neliecināja par klīniski nozīmīgu ietekmi uz imatiniba iedarbību. Analīze apstiprināja, ka imatiniba iedarbība bērniem, kuri saņēma 260 mg / m2 vienu reizi dienā (nepārsniedzot 400 mg vienu reizi dienā) vai 340 mg / m2 vienu reizi dienā (nepārsniedzot 600 mg vienu reizi dienā), bija līdzīga kā pieaugušiem pacientiem, kuri saņēma 400 mg imatiniba vai 600 mg vienu reizi dienā. Orgānu funkcijas traucējumi Imatinibs un tā metabolīti netiek būtiski izdalīti caur nierēm. Pacientiem ar viegliem un vidēji smagiem nieru darbības traucējumiem ir lielāka plazmas iedarbība nekā pacientiem ar normālu nieru darbību. Pieaugums ir aptuveni 1,5 līdz 2 reizes, kas atbilst 1,5 reizes lielākam plazmas AGP pieaugumam, kuram imatinibs spēcīgi saistās. Imatiniba kā brīvu zāļu klīrenss, visticamāk, būs līdzīgs pacientiem ar nieru darbības traucējumiem un normāls. izdalīšanās caur nierēm ir tikai neliels imatiniba eliminācijas ceļš (skatīt 4.2. un 4.4. apakšpunktu). Lai gan farmakokinētiskās analīzes rezultāti parādīja, ka indivīdiem ir būtiskas atšķirības, vidējā imatiniba iedarbība nepalielinājās pacientiem ar dažādas pakāpes aknu darbības traucējumiem, salīdzinot ar pacientiem ar normālu aknu darbību (skatīt 4.2., 4.4. Un 4.8. Apakšpunktu). Imatiniba preklīniskais drošības profils tika novērtēts pelēm, suņiem, pērtiķiem un trušiem. Vairāku devu toksicitātes pētījumi atklāja vieglas vai mērenas hematoloģiskas izmaiņas pelēm, suņiem un pērtiķiem, kam sekoja izmaiņas kaulu smadzenēs pelēm un suņiem. Aknas bija mērķa orgāns pelēm un suņiem. Abām sugām tika novērots neliels vai mērens transamināžu līmeņa paaugstināšanās un neliels holesterīna, triglicerīdu, kopējā proteīna un albumīna līmeņa pazemināšanās. Pelēm netika novērotas aknu histopatoloģiskas izmaiņas. Pelēm tika novērotas histopatoloģiskas aknu izmaiņas. Smags aknu toksicitātes līmenis suņiem, kas ārstēti 2 nedēļas, ar paaugstinātu aknu enzīmu vērtību, aknu šūnu nekrozi, nekrozi un žultsvadu hiperplāziju. Pērtiķiem, kuri tika ārstēti 2 nedēļas, tika konstatētas nieru toksicitātes parādības ar fokālu mineralizāciju un nieru kanāliņu paplašināšanos un tubulāro nefropātiju. Vairākiem no šiem dzīvniekiem tika novērots paaugstināts urīnvielas slāpekļa (BUN) un kreatinīna līmenis asinīs. 13 nedēļu pētījumā pelēm tika konstatēta pārejoša epitēlija hiperplāzija nieru papillā un urīnpūslī, lietojot devas ≥6 mg / kg. visas izmaiņas serumā un urīnā. Ilgstoši ārstējot imatinibu, tiek novērots oportūnistisku infekciju biežuma palielināšanās. 39 nedēļu ilgā pētījumā ar pērtiķiem netika konstatēts NOAEL (nenovērojamas nelabvēlīgas ietekmes līmenis) zemākajā devā 15 mg / kg, kas atbilst aptuveni trešdaļai maksimālās 800 mg devas cilvēkiem. aprēķina, pamatojoties uz ķermeņa virsmu. Terapija, kas tika veikta šiem dzīvniekiem, pasliktināja normāli nomāktas malārijas infekcijas. Imatinibu neuzskatīja par genotoksisku, pārbaudot baktēriju šūnu testā ES ielūdzu (Eimsa tests) ar "zīdītāju šūnu analīzi in vitro (peles limfoma) un ar peles mikrokodolu testu in vivo. Zīdītāju šūnu testā imatinibam tika iegūta pozitīva genotoksiska iedarbība in vitro (Ķīniešu kāmju olnīcas) klastogenitātes (hromosomu aberācijas) dēļ vielmaiņas aktivācijas klātbūtnē. Divi sagatavošanas procesa starpposma savienojumi, kas ir arī galaproduktā, izrādījās pozitīvi mutagēzes noteikšanā Ames testā, un viens no tiem bija arī pozitīvs peles limfomas analīzē. Auglības pētījumā, kas veikts ar peļu tēviņiem, devas aptuveni atbilst maksimālajai dienas klīniskajai devai 800 mg, kas noteikta, pamatojoties uz ķermeņa virsmas laukumu, ievadot 70 dienas pirms pārošanās, sēklinieku un epididima svara un kustīgo spermas procentuālais daudzums samazinājās līdz 60 mg / kg. Šī parādība netika konstatēta, lietojot devas ≤ 20 mg / kg. Nelielu vai mērenu spermatoģenēzes samazināšanos novēroja arī sunim, lietojot perorālās devas ≥30 mg / kg. Kad peļu mātītēm deva 14 dienas, pirms pārošanās un līdz sestajai grūtniecības dienai, ietekme uz pārošanos vai grūtniecību nebija. Lietojot 60 mg / kg devas, peļu mātītēm novēroja ievērojamu augļa zudumu pēc implantācijas un mazāk dzīvu augļu. Pirms un pēcdzemdību attīstības traucējumu pētījumā ar žurkām, lietojot perorāli, 45 mg / kg / dienā grupā tika novērota sarkana izdalīšanās no maksts 14. vai 15. grūtniecības dienā. Tajā pašā devā pieauga nedzīvi dzimušo skaits un subjekti, kas mira laikā no 0 līdz 4 dienām pēc dzemdībām. Tajā pašā devas līmenī F1 pēcnācējiem samazinājās vidējais ķermeņa svars no dzimšanas līdz galīgajai upurēšanai un nedaudz samazinājās to personu skaits, kas atbilst priekšādiņas atdalīšanas kritērijiem. F1 paaudzes auglība netika ietekmēta, bet, lietojot devu 45 mg / kg dienā, tika novērots rezorbciju skaita pieaugums un dzīvotspējīgu augļu skaita samazināšanās. Gan mātēm, gan F1 paaudzei nenovērojamais efekta līmenis (NOEL) bija 15 mg / kg dienā (viena ceturtdaļa no maksimālās 800 mg devas cilvēkiem). Imatinibs bija teratogēns pelēm, ja to ievadīja organoģenēzes laikā devās ≥100 mg / kg, kas ir aptuveni līdzvērtīga maksimālajai klīniskajai devai 800 mg dienā, ko nosaka ķermeņa virsmas laukums. frontālie kauli un parietālo kaulu neesamība Šīs sekas netika novērotas, lietojot devas ≤30 mg / kg. Attīstības toksikoloģijas pētījumā ar žurku mazuļiem (no 10. līdz 70. dienai pēc dzemdībām) netika identificēti jauni mērķa orgāni, salīdzinot ar zināmajiem mērķa orgāniem pieaugušām žurkām. Nepilngadīgo dzīvnieku toksikoloģijas pētījumā ietekme uz augšanu, aizkavēta maksts atvēršanās un priekšādiņas atdalīšanās tika novērota aptuveni 0,3-2 reizes vairāk nekā vidējā iedarbība bērniem, lietojot maksimālo ieteicamo devu 340 mg / m2. Turklāt mirstība tika novērota mazuļu dzīvniekiem (ap atšķiršanu), aptuveni 2 reizes pārsniedzot vidējo iedarbību bērniem, lietojot maksimālo ieteicamo devu 340 mg / m2. Divu gadu kancerogenitātes pētījumā ar žurkām, kuras tika ārstētas ar imatiniba devām 15, 30 un 60 mg / kg dienā, tika konstatēts statistiski nozīmīgs tēviņu ilgmūžības samazinājums, ārstējot ar 60 mg / kg / dienā, un mātītes, kuras tika ārstētas ar devām ≥30 mg / kg / dienā. Liemeņu histopatoloģiskā izmeklēšana atklāja kardiomiopātiju (abus dzimumus), hronisku progresējošu nefropātiju (sievietes) un priekšdziedzera papilomu kā galvenos nāves vai upurēšanas cēloņus. Neoplastisko izmaiņu mērķorgāni bija nieres, urīnpūslis, urīnizvadkanāls, priekšdziedzera un klitora dziedzeri, tievajās zarnās, parathormonos, virsnieru dziedzeros un kuņģī, kas nav dziedzeris. Lietojot devas, sākot no 30 mg / kg / dienā, ir novērotas priekšdziedzera un klitora dziedzeru papilomas / karcinomas, kas ir aptuveni 0,5 vai 0,3 reizes lielāka par cilvēka ekspozīciju, lietojot attiecīgi 400 mg / dienā vai 800 mg / dienā (pamatojoties uz AUC) un 0,4 reizes lielāka par dienas iedarbību bērniem, lietojot 340 mg / m2 dienā (pamatojoties uz AUC). Neievērojamās iedarbības līmenis (NOEL) bija 15 mg / kg dienā. Nieru adenoma / karcinoma, urīnpūšļa papiloma un urīnizvadkanālu, tievās zarnas adenokarcinomas, pieauss dziedzeru adenomas, labdabīgi un ļaundabīgi audzēji virsnieru medulārajā daļā un papilomas / karcinomas kuņģa ne dziedzeru daļā tika novērotas, lietojot 60 mg / kg dienā. ir aptuveni 1,7 vai 1 reizes lielāka par cilvēka ekspozīciju dienā, lietojot attiecīgi 400 mg vai 800 mg dienā (pamatojoties uz AUC), un 1,2 reizes dienā, lietojot 340 mg / m netika novērots efekts (NOEL) 30 mg / kg / dienā. Cilvēkiem šo atklājumu mehānisms un atbilstība žurku kanceroģenēzes pētījumā vēl nav noskaidrota. Iepriekšējos preklīniskajos pētījumos nav identificēti neoplastiski bojājumi, kas saistīti ar sirds un asinsvadu sistēmu, aizkuņģa dziedzeri, endokrīnajiem orgāniem un zobiem. Ievērojamākās izmaiņas bija sirds hipertrofija un paplašināšanās, kas dažiem dzīvniekiem izraisīja sirds mazspējas pazīmes. Aktīvā viela imatinibs rada risku videi nogulumu organismiem. Kapsulas saturs: mikrokristāliskā celuloze Krospovidons Magnija stearāts Koloidālais silīcija dioksīds, bezūdens Kapsulas apvalks: želatīns Dzeltenais dzelzs oksīds (E172) Titāna dioksīds (E171) Drukas tinte: sarkanais dzelzs oksīds (E172) Šellaks Sojas lecitīns Nav būtisks. 2 gadi Uzglabāt temperatūrā līdz 30 ° C. Uzglabāt oriģinālajā iepakojumā, lai pasargātu zāles no mitruma. PVC / alumīnija blisteris Iepakojumā 30 kapsulas. Neizlietotās zāles un šo zāļu atkritumi jāiznīcina saskaņā ar vietējiem noteikumiem. Novartis Europharm Limited Vimbblerstas ceļš Horsham Rietumsaseksa, RH12 5AB Lielbritānija EU/1/01/198/001 035372010 Reģistrācijas datums: 2001. gada 7. novembris Pēdējās pārreģistrācijas datums: 2006. gada 7. novembris 2014. gada jūlijs
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Glivec
Blakusparādības Kādas ir Glivec blakusparādības
Derīguma termiņš un saglabāšana
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija. 01.0 ZĀĻU NOSAUKUMS
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS
03.0 ZĀĻU FORMA
04.0 KLĪNISKĀ INFORMĀCIJA
04.1 Terapeitiskās indikācijas
04.2 Devas un lietošanas veids
HES / CEL (sākuma deva 100 mg) ANC 1. Pārtrauciet Glivec lietošanu, līdz ANC ≥ 1,5 x 109 / l un trombocīti ≥ 75 x 109 / l. 2. Atsākt ārstēšanu ar Glivec iepriekšējā devā (piemēram, pirms nopietnas blakusparādības). HML hroniska fāze, MDS / MPD un GIST (sākuma deva 400 mg) HES / CEL (400 mg deva) ANC 1. Pārtrauciet Glivec lietošanu, līdz ANC ≥ 1,5 x 109 / l un trombocīti ≥ 75 x 109 / l. 2. Atsākt ārstēšanu ar Glivec iepriekšējā devā (piemēram, pirms nopietnas blakusparādības). 3. ANC atkārtotas parādīšanās gadījumā HML hroniska fāze bērniem (deva 340 mg / m2) ANC 1. Pārtrauciet Glivec lietošanu, līdz ANC ≥ 1,5 x 109 / l un trombocīti ≥ 75 x 109 / l. 2. Atsākt ārstēšanu ar Glivec iepriekšējā devā (piemēram, pirms nopietnas blakusparādības). 3. Ja atkārtojas NCA 2. Paātrināta HML fāze un blastu krīze un Ph + ALL (sākuma deva 600 mg) aANC 1. Pārbaudiet, vai citopēnija ir saistīta ar leikēmiju (smadzeņu aspirācija vai biopsija). 2. Ja citopēnija nav saistīta ar leikēmiju, samaziniet Glivec devu līdz 400 mg. 3. Ja citopēnija saglabājas 2 nedēļas, samaziniet to līdz 300 mg. 4. Ja citopēnija saglabājas 4 nedēļas un joprojām nav saistīta ar leikēmiju, pārtrauciet Glivec lietošanu, līdz ANC ir ≥ 1 x 109 / l un trombocīti ≥ 20 x 109 / l, un pēc tam atsākiet ārstēšanu ar 300 mg devu. Paātrinātā CML pediatriskā fāze un blastu krīze (sākuma deva 340 mg / m2) aANC 1. Pārbaudiet, vai citopēnija ir saistīta ar leikēmiju (kaulu smadzeņu aspirācija vai biopsija). 2. Ja citopēnija nav saistīta ar leikēmiju, samaziniet Glivec devu līdz 260 mg / m2. 3. Ja citopēnija saglabājas 2 nedēļas, samaziniet to līdz 200 mg / m2. 4. Ja citopēnija saglabājas 4 nedēļas un joprojām nav saistīta ar leikēmiju, pārtrauciet Glivec lietošanu, līdz ANC ir ≥ 1 x 109 / l un trombocīti ≥ 20 x 109 / l, un pēc tam atsākiet ārstēšanu ar 200 mg / m2. DFSP (deva 800 mg) ANC 1. Pārtrauciet Glivec lietošanu, līdz ANC ≥ 1,5 x 109 / l un trombocīti ≥ 75 x 109 / l. 2. Atsākt ārstēšanu ar Glivec 600 mg devā. 3. ANC atkārtotas parādīšanās gadījumā ANC = absolūtais neitrofilu skaits
sāpes rodas pēc vismaz 1 mēneša ārstēšanas Aknu disfunkcija Aknu funkcijas analīze Viegla Kopējais bilirubīns: = 1,5 ULN AST:> ULN (var būt normāls vai ULN) Mērens Kopējais bilirubīns:> 1,5-3,0 ULN AST: jebkurš Nopietni Kopējais bilirubīns:> 3-10 ULN
AST: jebkurš
04.3 Kontrindikācijas
04.4 Īpaši brīdinājumi un piesardzība lietošanā
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi
04.6 Grūtniecība un zīdīšana
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
04.8 Nevēlamās blakusparādības
Infekcijas un invāzijas Retāk: Herpes zoster, herpes simplex, nazofaringīts, pneimonija1, sinusīts, celulīts, augšējo elpceļu infekcija, gripa, urīnceļu infekcija, gastroenterīts, sepsis Reti: Sēnīšu infekcija Labdabīgi, ļaundabīgi un neprecizēti jaunveidojumi (ieskaitot cistas un polipus) Reti: Audzēja līzes sindroms Asins un limfātiskās sistēmas traucējumi Ļoti bieži sastopams: Neitropēnija, trombocitopēnija, anēmija Bieži: Pancitopēnija, febrilā neitropēnija Retāk: Trombocitēmija, limfopēnija, kaulu smadzeņu nomākums, eozinofīlija, limfadenopātija Reti: Hemolītiskā anēmija Vielmaiņas un uztura traucējumi Bieži: Anoreksija Retāk: Hipokaliēmija, palielināta ēstgriba, hipofosfatēmija, samazināta ēstgriba, dehidratācija, podagra, hiperurikēmija, hiperkalciēmija, hiperglikēmija, hiponatriēmija Reti: Hiperkaliēmija, hipomagnēmija Psihiskie traucējumi Bieži: Bezmiegs Retāk: Depresija, samazināts libido, trauksme Reti: Apjukuma stāvoklis Nervu sistēmas traucējumi Ļoti bieži sastopams: Galvassāpes 2 Bieži: Reibonis, parestēzija, garšas traucējumi, hipestēzija Retāk: Migrēna, miegainība, ģībonis, perifēra neiropātija, atmiņas traucējumi, išiass, nemierīgo kāju sindroms, trīce, smadzeņu asiņošana Reti: Paaugstināts intrakraniālais spiediens, krampji, redzes neirīts Acu slimības Bieži: Plakstiņu tūska, pastiprināta asarošana, konjunktīvas asiņošana, konjunktivīts, sausa acs, neskaidra redze Retāk: Acu kairinājums, sāpes acīs, orbitāla tūska, asiņošana no sklēras, tīklenes asiņošana, blefarīts, makulas tūska Reti: Katarakta, glaukoma, papiljēma Ausu un labirinta traucējumi Retāk: Vertigo, troksnis ausīs, dzirdes zudums Sirds patoloģijas Retāk: Sirdsklauves, tahikardija, sastrēguma sirds mazspēja3, plaušu tūska Reti: Aritmija, priekškambaru mirdzēšana, sirdsdarbības apstāšanās, miokarda infarkts, stenokardija, perikarda izsvīdums Asinsvadu sistēmas traucējumi 4 Bieži: Sārtums, asiņošana Retāk: Hipertensija, hematoma, subdurāla hematoma, ekstremitāšu dzesēšana, hipotensija, Reino fenomens Elpošanas, krūšu kurvja un videnes slimības Bieži: Elpas trūkums, deguna asiņošana, klepus Retāk: Pleiru izsvīdums5, rīkles sāpes, faringīts Reti: Pleirītiskas sāpes, plaušu fibroze, plaušu hipertensija, plaušu asiņošana Kuņģa -zarnu trakta traucējumi Ļoti bieži sastopams: Slikta dūša, caureja, vemšana, dispepsija, sāpes vēderā 6 Bieži: Meteorisms, vēdera uzpūšanās, gastroezofageālais reflukss, aizcietējums, sausa mute, gastrīts Retāk: Stomatīts, čūlas mutē, kuņģa -zarnu trakta asiņošana7, atraugas, melēna, ezofagīts, ascīts, kuņģa čūla, hematemēze, heilīts, disfāgija, pankreatīts Reti: Kolīts, ileuss, iekaisīga zarnu slimība Aknu un žultsceļu darbības traucējumi Bieži: Paaugstināts aknu enzīmu līmenis Retāk: Hiperbilirubinēmija, hepatīts, dzelte Reti: Aknu mazspēja8, aknu nekroze Ādas un zemādas audu bojājumi Ļoti bieži sastopams: Periorbitāla tūska, dermatīts / ekzēma / izsitumi Bieži: Nieze, sejas tūska, sausa āda, eritēma, alopēcija, svīšana naktī, fotosensitivitātes reakcijas Retāk: Pustulāri izsitumi, sasitumi, pastiprināta svīšana, nātrene, ekhimoze, palielināta nosliece uz zilumiem, hipotrichoze, ādas hipopigmentācija, eksfoliatīvs dermatīts, onihoklāze, folikulīts, petehijas, psoriāze, purpura, ādas hiperpigmentācija, bullozi izvirdumi Reti: Akūta febrilā neitrofīlā dermatoze (Svīta sindroms), nagu krāsas izmaiņas, angioneirotiskā tūska, vezikulāri izsitumi, daudzformāla eritēma, leikocitoklastiskais vaskulīts, Stīvensa-Džonsona sindroms, akūta ģeneralizēta eksantemātiska pustuloze (AGEP) Skeleta -muskuļu un saistaudu sistēmas bojājumi Ļoti bieži sastopams: Muskuļu spazmas un krampji, muskuļu un skeleta sāpes, ieskaitot mialģiju, artralģiju, kaulu sāpes9 Bieži: Locītavu pietūkums Retāk: Locītavu un muskuļu stīvums Reti: Muskuļu vājums, artrīts, rabdomiolīze / miopātija Nieru un urīnceļu traucējumi Retāk: Nieru sāpes, hematūrija, akūta nieru mazspēja, pollakurija Reproduktīvās sistēmas un krūts slimības Retāk: Ginekomastija, erektilā disfunkcija, menorāģija, neregulāras menstruācijas, seksuāla disfunkcija, sāpes sprauslas, krūšu palielināšanās, sēklinieku tūska Reti: Hemorāģiskais dzeltenais ķermenis / hemorāģiskā olnīcu cista Vispārēji traucējumi un reakcijas ievadīšanas vietā Ļoti bieži sastopams: Ūdens aizture un tūska, nogurums Bieži: Vājums, drudzis, anasarka, drebuļi, trīce Retāk: Sāpes krūtīs, savārgums Diagnostikas testi Ļoti bieži sastopams: Svara pieaugums Bieži: Svara zudums Retāk: Paaugstināts kreatinīna līmenis asinīs, paaugstināts kreatīna fosfokināzes līmenis asinīs, palielināts laktāta dehidrogenāzes līmenis asinīs, palielināts sārmainās fosfatāzes līmenis asinīs
Reti: Paaugstināta amilāzes koncentrācija asinīs Labdabīgi, ļaundabīgi un neprecizēti jaunveidojumi (ieskaitot cistas un polipus) Nezinams: Audzēja asiņošana / audzēja nekroze Imūnsistēmas traucējumi Nezinams: Anafilaktiskais šoks Nervu sistēmas traucējumi Nezinams: Smadzeņu tūska Acu slimības Nezinams: Stiklveida asiņošana Sirds patoloģijas Nezinams: Perikardīts, sirds tamponāde Asinsvadu patoloģijas Nezinams: Tromboze / embolija Elpošanas, krūšu kurvja un videnes slimības Nezinams: Akūta elpošanas mazspēja1, intersticiāla plaušu slimība Kuņģa -zarnu trakta traucējumi Nezinams: Ileuss / zarnu aizsprostojums, kuņģa -zarnu trakta perforācija, divertikulīts Ādas un zemādas audu bojājumi Nezinams: Plaukstas-plantāra eritrodizestēzijas sindroms Nezinams: Ķērpju keratoze, plānais ķērpis Nezinams: Toksiska epidermas nekrolīze Nezinams: Ādas zāļu reakcija ar eozinofīliju un sistēmiskiem simptomiem (DRESS) Skeleta -muskuļu un saistaudu sistēmas bojājumi Nezinams: Avaskulāra nekroze / gūžas nekroze
Nezinams: Augšanas aizkavēšanās bērniem
04.9 Pārdozēšana
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS
05.1 Farmakodinamiskās īpašības
(Labākie atbildes rādītāji) Glivec n = 553 IFN + Ara-C n = 553 Hematoloģiskā reakcija REC n (%) 534(96,6%)* 313 (56,6%)* [95% TI] [94,7%, 97,9%] [52,4%, 60,8%] Citoģenētiskā reakcija Galvenā atbilde n (%) 490 (88,6%)* 129 (23,3%)* [95% TI] [85,7%, 91,1%] [19,9%, 27,1%] Pabeigt CyR n (%) 456 (82,5%)* 64 (11,6%)* Daļējs CyR n (%) 34 (6,1%) 65 (11,8%) Molekulārā reakcija ** Galvenā atbilde pēc 12 mēnešiem (%) 153/305=50,2% 8/83=9,6% Galvenā atbilde pēc 24 mēnešiem (%) 73/104=70,2% 3/12=25%
Galvenā reakcija pēc 84 mēnešiem (%) 102/116=87,9% 3/4=75% Pētījums 0110 37 mēnešu dati Hroniska fāze, IFN mazspēja (n = 532) Pētījuma 0109 dati pēc 40,5 mēnešiem Paātrinātā fāze (n = 235) Pētījums 0102 38 mēnešu dati Mieloīdā sprādziena krīze (n = 260) % pacientu (95% TI) Hematoloģiskā reakcija 1 95% (92,3-96,3) 71% (65,3-77,2) 31% (25,2-36,8) Pilnīga hematoloģiskā reakcija (REC) 95% 42% 8% Nav pierādījumu par leikēmiju (NEL) Nav būtisks 12% 5% Atgriešanās hroniskajā fāzē (RFC) Nav būtisks 17% 18% Galvenā citoģenētiskā reakcija 2 65% (61,2-69,5) 28% (22,0-33,9) 15% (11,2-20,4) Pabeigts 53% 20% 7% (Apstiprināts3) [95% TI] (43%) [38,6-47,2] (16%) [11,3-21,01] (2%) [0,6-4,4] Daļēji 12% 7% 8% 1 Hematoloģiskās atbildes reakcijas kritēriji (visas atbildes jāapstiprina pēc ≥ 4 nedēļām): REC Studio 0110 [WBC NEL Tādi paši kritēriji kā REC, bet ANC ≥ 1 x 109 / l un trombocīti ≥ 20 x 109 / l (tikai 0102 un 0109) Liesa un aknu RFC (tikai 0102 un 0109). MO = kaulu smadzenes, SP = perifērās asinis 2 Citoģenētiskās atbildes kritēriji: atbilstoša reakcija apvieno gan pilnīgas, gan daļējas atbildes: pilnīga (0% P Ph + metafāzes), daļēja (1-35%).
3 Pilnīga citoģenētiskā reakcija, ko apstiprina otrā kaulu smadzeņu citoģenētiskā izmeklēšana, kas veikta vismaz reizi mēnesī pēc sākotnējās kaulu smadzeņu aptaujas. Pētījums ADE10 Priekšapstrāde DEX 10 mg / m2 iekšķīgi, 1.-5. CP 200 mg / m2 i.v., 3., 4., 5. diena; MTX 12 mg intratekāli, 1. diena Indukcija DEX 10 mg / m2 iekšķīgi, 6.-7., 13.-16. Videomagnetofons 1 mg i.v., 7., 14. diena; IDA 8 mg / m2 i.v. (0,5 h), 7., 8., 14., 15. diena; CP 500 mg / m2 i.v. (1 h) 1. diena; Ara-C 60 mg / m2 i.v., 22.-25., 29.-32 Konsolidācija I, III, V MTX 500 mg / m2 i.v. (24 stundas), 1., 15. diena; 6-MP 25 mg / m2 iekšķīgi, 1.-20 Konsolidācija II, IV Ara-C 75 mg / m2 i.v. (1 h), 1.-5. Diena; VM & SUP2; 6 60 mg / m2 i.v. (1 h), 1.-5. Diena Pētījums AAU02 Indukcija (de novo Ph + ALL) Daunorubicīns 30 mg / m2 i.v., 1., 3., 15.-16. Diena; VCR kopējā deva 2 mg i.v., 1., 8., 15., 22. diena; CP 750 mg / m2 i.v., 1., 8. diena; Prednizons 60 mg / m2 iekšķīgi, 1.-7., 15.-21. IDA 9 mg / m2 iekšķīgi, 1-28 dienas; MTX 15 mg intratekāli, 1., 8., 15., 22. diena; Ara-C 40 mg intratekāli, 1., 8., 15., 22. diena; Metilprednizolons 40 mg intratekāli, 1., 8., 15., 22. diena Konsolidācija (de novo Ph + ALL) Ara-C 1000 mg / m2 / 12 h i.v. (3 h), 1.-4. Diena; Mitoksantrons 10 mg / m2 i.v. 3-5 dienas; MTX 15 mg intratekāli, 1. diena; Metilprednizolons 40 mg intratekāli, 1. diena Pētījums ADE04 Priekšapstrāde DEX 10 mg / m2 iekšķīgi, 1.-5. CP 200 mg / m2 i.v., 3-5 dienas; MTX 15 mg intratekāli, 1. diena Indukcija I DEX 10 mg / m2 iekšķīgi, 1.-5. VCR 2 mg i.v., 6., 13., 20. diena; Daunorubicīns 45 mg / m2 i.v., 6.-7., 13.-14 Indukcija II KP 1 g / m2 i.v. (1 h), 26., 46. diena; Ara-C 75 mg / m2 i.v. (1 h), 28. – 31., 35. – 38., 42. – 45. Diena; 6-MP 60 mg / m2 iekšķīgi, 26.-46 Konsolidācija DEX 10 mg / m2 iekšķīgi, 1.-5. Vindesīns 3 mg / m2 i.v., 1. diena; MTX 1,5 g / m2 i.v. (24 stundas), 1. diena; Etopozīds 250 mg / m2 i.v. (1 h) 4-5 dienas; Ara-C 2x 2 g / m2 i.v. (3 h, q 12 h), 5. diena Pētījums AJP01 Indukcija KP 1,2 g / m2 i.v. (3 h), 1. diena; Daunorubicīns 60 mg / m2 i.v. (1 h), 1.-3. Diena; Vinkristīns 1,3 mg / m2 i.v., 1., 8., 15., 21. diena; Prednizolons 60 mg / m2 dienā perorāli Konsolidācija Alternatīvs ķīmijterapijas kurss: lielas devas MTX ķīmijterapija 1 g / m2 i.v. (24 stundas), 1. diena, un Ara-C 2 g / m2 i.v. (q 12 h), 2-3 dienas, 4 cikliem Apkope Videomagnetofons 1,3 g / m2 i.v., 1. diena; Prednizolons 60 mg / m2 iekšķīgi, 1.-5 Pētījums AUS01 Indukcija-konsolidācija Hyper-CVAD dozēšanas grafiks: CP 300 mg / m2 i.v. (3 h, q 12 h), 1.-3. Diena; Vinkristīns 2 mg i.v., 4., 11. diena; Doksorubicīns 50 mg / m2 i.v. (24 stundas), 4. diena; DEX 40 mg / dienā 1.-4. Un 11.-14. Dienā, pārmaiņus ar MTX 1 g / m2 i.v. (24 stundas), 1. diena, Ara-C 1 g / m2 i.v. (2 h, q 12 h), 2-3 dienas (kopā 8 cikli) Apkope VCR 2 mg i.v. reizi mēnesī 13 mēnešus; Prednizolons 200 mg iekšķīgi, 5 dienas mēnesī 13 mēnešus Visas ārstēšanas shēmas ietver steroīdu ievadīšanu CNS profilaksei.
Ara-C: citarabīns; CP: ciklofosfamīds; DEX: deksametazons; MTX: metotreksāts; 6-MP: 6-merkaptopurīns; VM & SUP2; 6: tenipozīds; Videomagnetofons: vinkristīna; IDA: idarubicīns; i.v .: intravenozi Konsolidācijas bloks 1 (3 nedēļas) VP-16 (100 mg / m2 / dienā, IV): 1.-5 Ifosfamīds (1,8 g / m2 / dienā, IV): 1.-5 MESNA (360 mg / m2 / deva ik pēc 3 stundām, x 8 devas dienā, IV): 1.-5 G-CSF (5 mcg / kg, SC): 6.-15. Diena vai līdz ANC> 1500 pēc zemākā līmeņa Metotreksāts IT (pielāgots vecumam): IESLĒGTA 1. diena Trīskārša IT terapija (pielāgots vecumam): 8., 15. diena 2. konsolidācijas bloks (3 nedēļas) Metotreksāts (5 g / m2 24 stundas, IV): 1. diena Leukovorīns (75 mg / m2 36 stundās, IV; 15 mg / m2 IV vai PO 6 stundas x 6 devas) iii: 2. un 3. diena Trīskārša IT terapija (pielāgots vecumam): 1. diena ARA-C (3 g / m2 / deva q 12 h x 4, IV): 2. un 3. diena G-CSF (5 mcg / kg, SC): 4.-13. Diena vai līdz ANC> 1500 pēc zemākā līmeņa Atkārtotas indukcijas 1. bloks (3 nedēļas) VCR (1,5 mg / m2 / dienā, IV): 1., 8. un 15. diena DAUN (45 mg / m2 / dienā bolus, IV): 1. un 2. diena CPM (250 mg / m2 / deva ik pēc 12 stundām x 4 devas, IV): 3. un 4. diena PEG-ASP (2500 SV / m2, IM): 4. diena G-CSF (5 mcg / kg, SC): 5.-14. Diena vai līdz ANC> 1500 pēc zemākā līmeņa Trīskārša IT terapija (pielāgots vecumam): 1. un 15. diena DEX (6 mg / m2 / dienā, PO): 1.-7. Un 15.-21 Pastiprinājuma 1. bloks (9 nedēļas) Metotreksāts (5 g / m2 24 stundas, IV): 1. un 15. diena Leikovorīns (75 mg / m2 36 stundās, IV; 15 mg / m2 IV vai PO 6 stundas x 6 devas) iii: 2., 3., 16. un 17. diena Trīskārša IT terapija (pielāgots vecumam): 1. un 22. diena VP-16 (100 mg / m2 / dienā, IV): 22.-26 MPT (300 mg / m2 / dienā, IV): 22.-26 MESNA (150 mg / m2 / dienā, IV): 22.-26 G-CSF (5 mcg / kg, SC): 27. – 36. Diena vai līdz ANC> 1500 pēc zemākā līmeņa ARA-C (3 g / m2, ik 12 stundas, IV): 43., 44. diena L-ASP (6000 SV / m2, IM): 44. diena Reindukcijas 2. bloks (3 nedēļas) VCR (1,5 mg / m2 / dienā, IV): 1., 8. un 15. diena DAUN (45 mg / m2 / dienā bolus, IV): 1. un 2. diena CPM (250 mg / m2 / deva ik pēc 12 stundām x 4 devas, iv): 3. un 4. diena PEG-ASP (2500 SV / m2, IM): 4. diena G-CSF (5 mcg / kg, SC): 5.-14. Diena vai līdz ANC> 1500 pēc zemākā līmeņa Trīskārša IT terapija (pielāgots vecumam): 1. un 15. diena DEX (6 mg / m2 / dienā, PO): 1.-7. Un 15.-21 2. intensifikācijas bloks (9 nedēļas) Metotreksāts (5 g / m2 24 stundas, IV): 1. un 15. diena Leikovorīns (75 mg / m2 36 stundās, IV; 15 mg / m2 IV vai PO 6 stundas x 6 devas) iii: 2., 3., 16. un 17. diena Trīskārša IT terapija (pielāgots vecumam): 1. un 22. diena VP-16 (100 mg / m2 / dienā, IV): 22.-26 MPT (300 mg / m2 / dienā, IV): 22.-26 MESNA (150 mg / m2 / dienā, IV): 22.-26 G-CSF (5 mcg / kg, SC): 27. – 36. Diena vai līdz ANC> 1500 pēc zemākā līmeņa ARA-C (3 g / m2, ik 12 stundas, IV): 43., 44. diena L-ASP (6000 SV / m2, IM): 44. diena Apkope (8 nedēļu cikli) 1.-4 MTX (5 g / m2 24 stundas, IV): 1. diena Leukovorīns (75 mg / m2 36 stundās, IV; 15 mg / m2 IV vai PO 6 stundas x 6 devas) iii: 2. un 3. diena Trīskārša IT terapija (pielāgots vecumam): 1., 29. diena VCR (1,5 mg / m2, IV): 1., 29. diena DEX (6 mg / m2 / dienā PO): dienas 1-5; 29-33 6 MP (75 mg / m2 / dienā, PO): 8.-28. Diena Metotreksāts (20 mg / m2 / nedēļā, PO): 8., 15., 22. diena VP-16 (100 mg / m2, IV): 29.-33 MPT (300 mg / m2, IV): 29.-33 IV MĒNESIS 29.-33. Diena G-CSF (5 mcg / kg, SC): 34.-43. Diena Apkope (8 nedēļu cikli) 5. cikls Galvaskausa apstarošana (tikai 5. bloks) 12 Gy 8 frakcijās visiem pacientiem, kuriem diagnozes laikā ir CNS1 un CNS2 18 Gy 10 frakcijās visiem pacientiem, kuriem diagnozes laikā ir CNS3 VCR (1,5 mg / m2 / dienā, IV): 1., 29. diena DEX (6 mg / m2 / dienā, PO): dienas 1-5; 29-33 6-MP (75 mg / m2 / dienā, PO): 11.-56. Diena (aizturiet 6-MP 6-10. Dienā, kad galvaskausa apstarošana sākās 5. cikla 1. dienā. Sāciet 6-MP pirmajā dienā pēc kursa pabeigšanas galvaskausa apstarošana.) Metotreksāts (20 mg / m2 nedēļā, PO): 8., 15., 22., 29., 36., 43., 50. diena Apkope (8 nedēļu cikli) 6.-12 VCR (1,5 mg / m2 / dienā, IV): 1., 29. diena DEX (6 mg / m2 / dienā, PO): dienas 1-5; 29-33 6 MP (75 mg / m2 / dienā, PO): dienas 1-56
Metotreksāts (20 mg / m2 nedēļā, PO): 1., 8., 15., 22., 29., 36., 43., 50. diena Labākā atbilde Visas devas (n = 147) 400 mg (n = 73) 600 mg (n = 74) n (%) Pilnīga atbilde 1 Daļēja atbilde 98 Stabila slimība 23 Slimības progresēšana 18 Nav vērtējams 5
Nezināms 2 Riska kritēriji Riska klase % pacientu Notikumu skaits / Nr. no pacientiem Kopējā bīstamības attiecība (95% TI) * RFS vērtības (%) 12 mēneši 24 mēneši Glivec vs. placebo Glivec vs. placebo Glivec vs. placebo NIH Bass 29,5 0/86 pret. 2/90 N.S. 100 pret. 98.7 100 pret. 95.5 Vidējs 25,7 4/75 pret. 6/78 0,59 (0,17; 2,10) 100 pret. 94.8 97,8 pret. 89,5 Garš 44,8 21/140 pret. 51/127 0,29 (0,18; 0,49) 94,8 pret. 64.0 80,7 pret. 46.6 AFIP Ļoti zems 20,7 0/52 pret. 2/63 N.S. 100 pret. 98.1 100 pret. 93,0 Bass 25,0 2/70 pret. 0/69 N.S. 100 pret. 100 97,8 pret. 100 Mērens 24,6 2/70 pret. 11/67 0,16 (0,03; 0,70) 97,9 pret. 90.8 97,9 pret. 73.3
Garš 29,7 16/84 pret. 39/81 0,27 (0,15; 0,48) 98,7 pret. 56.1 79,9 pret. 41.5 RFS 12 mēnešu ārstēšanas grupa% (TI) 36 mēnešu ārstēšanas grupa% (TI) 12 mēneši 93,7 (89,2-96,4) 95,9 (91,9-97,9) 24 mēneši 75,4 (68,6-81,0) 90,7 (85,6-94,0) 36 mēneši 60,1 (52,5-66,9) 86,6 (80,8-90,8) 48 mēneši 52,3 (44,0-59,8) 78,3 (70,8-84,1) 60 mēneši 47,9 (39,0-56,3) 65,6 (56,1-73,4) Izdzīvošana 36 mēneši 94,0 (89,5-96,7) 96,3 (92,4-98,2) 48 mēneši 87,9 (81,1-92,3) 95,6 (91,2-97,8)
60 mēneši 81,7 (73,0-87,8) 92,0 (85,3-95,7)
05.2 "Farmakokinētiskās īpašības
05.3 Preklīniskie drošības dati
06.0 FARMACEITISKĀ INFORMĀCIJA
06.1 Palīgvielas
06.2 Nesaderība
06.3 Derīguma termiņš
06.4 Īpaši uzglabāšanas nosacījumi
06.5 Tiešā iepakojuma veids un iepakojuma saturs
06.6 Norādījumi lietošanai un lietošanai
07.0 REĢISTRĀCIJAS APLIECĪBAS ĪPAŠNIEKS
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS
11.0 RADIOZĀLĒM, PILNĪGI DATI PAR IEKŠĒJO RADIĀCIJAS DOSIMETRIJU
12.0 RADIOZĀLĒM, PAPILDU SĪKĀKI NORĀDĪJUMI PAR ĪSTENAJU SAGATAVOŠANU UN KVALITĀTES KONTROLI










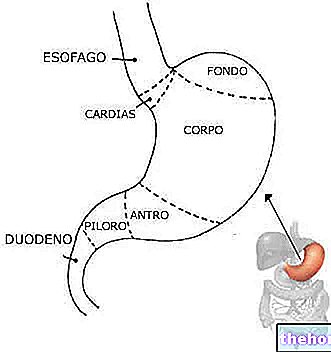
















.jpg)