Aktīvās sastāvdaļas: Tamsulosīns (Tamsulozīna hidrohlorīds)
Pradif 0,4 mg cietās kapsulas ar modificētu darbību
Kāpēc lieto Pradif? Kam tas paredzēts?
Pradif aktīvā viela ir tamsulozīns, selektīvs α1A / α1D antagonists, kas samazina muskuļu sasprindzinājumu prostatā un urīnizvadkanālā. Tas ļauj urīnam ātrāk izplūst caur urīnizvadkanālu, atvieglojot urinēšanu. Tas samazina urinēšanas steidzamības sajūtu.
Pradif lieto vīriešiem, lai ārstētu apakšējo urīnceļu simptomus, kas saistīti ar prostatas palielināšanos (labdabīga prostatas hiperplāzija). Šie traucējumi var ietvert apgrūtinātu urinēšanu (strūklas sašaurināšanos), pilēšanu, steidzamību un urinēšanas biežuma palielināšanos. dienu un nakti.
Kontrindikācijas Kad Pradif nedrīkst lietot
Nelietojiet Pradif
- ja Jums ir alerģija (paaugstināta jutība) pret tamsulosīnu vai kādu citu Pradif sastāvdaļu. Paaugstināta jutība var izpausties kā pēkšņs ķermeņa mīksto audu (piemēram, rīkles vai mēles) pietūkums, apgrūtināta elpošana un / vai nieze un izsitumi (angioneirotiskā tūska),
- ja Jums ir smagi aknu darbības traucējumi,
- ja, samainoties pozīcijām (apsēžoties vai pieceļoties), noģībst asinsspiediens.
Piesardzība lietošanā Kas jāzina pirms Pradif lietošanas
Īpaša piesardzība, lietojot Pradif, nepieciešama šādos gadījumos
- Nepieciešamas periodiskas medicīniskās pārbaudes, lai uzraudzītu, kā attīstās stāvoklis, kura dēļ jūs ārstējaties.
- Reti, lietojot Pradif, tāpat kā citas šāda veida zāles, var rasties ģībonis.Pēc pirmajām reiboņa vai vājuma pazīmēm jums vajadzētu sēdēt vai apgulties, līdz tās pazūd.
- Ja Jums ir smagi nieru darbības traucējumi, lūdzu, pastāstiet savam ārstam.
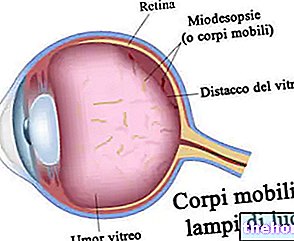
- Ja Jums tiek veikta vai plānota acu operācija lēcas apduļķošanās dēļ (katarakta) vai paaugstināts acs spiediens (glaukoma). Pastāstiet savam oftalmologam, ja esat iepriekš lietojis, lietojat vai plānojat lietot Pradif. Tādējādi speciālists var veikt vispiemērotākos piesardzības pasākumus attiecībā uz zālēm un izmantojamo ķirurģisko tehniku. Jautājiet savam ārstam, vai Jums vajadzētu atlikt vai īslaicīgi pārtraukt ārstēšanu ar Pradif, pirms veicat acu operāciju lēcas apduļķošanās (katarakta) vai paaugstināta acs spiediena (glaukoma) dēļ.
Bērni
Nedodiet šīs zāles bērniem vai pusaudžiem, kas jaunāki par 18 gadiem, jo šīs grupas pacientiem tās nav efektīvas.
Mijiedarbība Kādas zāles vai pārtikas produkti var mainīt Pradif iedarbību
Pradif lietošana kopā ar citām zālēm
Pradif lietošana kopā ar citām tās pašas klases zālēm (α1-adrenoreceptoru antagonisti) var izraisīt nevēlamu asinsspiediena pazemināšanos, Pradif no organisma (piemēram, ketokonazolu, eritromicīnu).
Pastāstiet ārstam vai farmaceitam par visām zālēm, kuras lietojat vai pēdējā laikā esat lietojis, ieskaitot zāles, ko var iegādāties bez receptes.
Pradif lietošana kopā ar uzturu
Pradif jālieto pēc brokastīm vai pirmās ēdienreizes dienā
Brīdinājumi Ir svarīgi zināt, ka:
Grūtniecība, zīdīšanas periods un auglība
Pradif nav indicēts lietošanai sievietēm.
Vīrietim ziņots par patoloģisku ejakulāciju (ejakulācijas traucējumiem). Tas nozīmē, ka sēklas šķidrums neiziet no ķermeņa caur urīnizvadkanālu, bet iekļūst urīnpūslī (retrogrāda ejakulācija) vai ka ejakulācijas tilpums ir samazināts vai nav vispār (ejakulācijas mazspēja). Šis notikums ir nekaitīgs.
Transportlīdzekļu vadīšana un mehānismu apkalpošana
Nav pierādīts, ka Pradif ietekmē spēju vadīt transportlīdzekļus vai apkalpot mehānismus vai aprīkojumu. Tomēr jums jāpatur prātā iespēja, ka var rasties reibonis, un tādā gadījumā jūs nedrīkstat veikt darbības, kurām jāpievērš uzmanība.
Deva, lietošanas veids un laiks Kā lietot Pradif: Devas
Vienmēr lietojiet Pradif tieši tā, kā ārsts Jums stāstījis. Ja neesat pārliecināts, konsultējieties ar ārstu vai farmaceitu. Parastā deva ir 1 kapsula dienā, kas jālieto pēc brokastīm vai pēc dienas pirmās ēdienreizes.
Kapsula jānorij vesela, nesasmalcinot vai košļājot.
Pradif parasti tiek parakstīts uz ilgu laiku. Ietekme uz urīnpūsli un urinēšanu saglabājas pēc ilgstošas ārstēšanas ar Pradif.
Pārdozēšana Ko darīt, ja esat lietojis pārāk daudz Pradif
Ja esat lietojis Pradif vairāk nekā noteikts
Pārāk daudz Pradif lietošanas var izraisīt nevēlamu asinsspiediena pazemināšanos un sirdsdarbības ātruma palielināšanos, kas saistīta ar vājuma sajūtu.Ja esat lietojis pārāk daudz Pradif devu, nekavējoties konsultējieties ar ārstu.
Ja esat aizmirsis lietot Pradif
Ja esat aizmirsis lietot Pradif devu, varat to lietot vēlāk. Ja esat izlaidis dienu, turpiniet lietot dienas kapsulu parastajā laikā.Nekad nelietojiet dubultu devu, lai aizvietotu aizmirsto.
Ja pārtraucat lietot Pradif
Ja ārstēšana ar Pradif tiek pārtraukta priekšlaicīgi, sākotnējie simptomi var parādīties no jauna. Tāpēc turpiniet lietot Pradif tik ilgi, cik ārsts Jums teicis, pat ja simptomi jau ir pazuduši. Vienmēr konsultējieties ar ārstu, ja uzskatāt, ka šī terapija jāpārtrauc.
Ja jums ir kādi jautājumi par šo zāļu lietošanu, jautājiet savam ārstam vai farmaceitam.
Blakusparādības Kādas ir Pradif blakusparādības
Tāpat kā citas zāles, Pradif var izraisīt blakusparādības, kaut arī ne visiem tās izpaužas.
Biežas sekas (mazāk nekā 1 no 10 gadījumiem, vairāk nekā 1 no 100 gadījumiem (1-10%)):
reibonis, īpaši sēžot vai pieceļoties.
Nenormāla ejakulācija (ejakulācijas traucējumi). Šis simptoms nozīmē, ka sēklas šķidrums neizplūst no ķermeņa caur urīnizvadkanālu, bet iekļūst urīnpūslī (retrogrāda ejakulācija) vai ka sēklas šķidruma tilpums ir samazināts vai nav vispār (ejakulācijas mazspēja). ir nekaitīgs.
Retākas blakusparādības (vairāk nekā 1 gadījums no 1000, mazāk nekā 1 gadījums no 100 (0,1-1%)):
galvassāpes, sirdsklauves (sirds pukst biežāk nekā parasti, un tas ir arī manāms), asinsspiediena pazemināšanās, piemēram, ātra piecelšanās no sēdēšanas vai guļus, bieži vien saistīta ar reiboni, aizliktu vai iesnas (iesnu), caureju, sliktu dūšu un vemšanu, aizcietējums, vājums (astēnija), ādas apsārtums (izsitumi), nieze un nātrene.
Retas blakusparādības (vairāk nekā 1 gadījums no 10 000, mazāk nekā 1 gadījums no 1000 (0,01–0,1%)):
ģībonis un pēkšņi lokalizēti ķermeņa mīksto audu (piemēram, rīkles un mēles) pietūkumi, apgrūtināta elpošana ar niezi vai bez tās un ādas apsārtums (izsitumi), kā bieži alerģiskas reakcijas gadījumā (angioedēma).
Ļoti reti sastopami efekti (mazāk nekā 1 gadījumam no 10 000 (<0,01%)):
priapisms (sāpīga un ilgstoša piespiedu erekcija, kurai nepieciešama tūlītēja medicīniska palīdzība). Izsitumi, iekaisums, pūslīši uz ādas un / vai lūpu, acu, mutes, nāsīs vai dzimumorgānos (Stīvensa-Džonsona sindroms).
Ietekme, kuras biežums nav zināms (biežumu nevar noteikt pēc pieejamiem datiem):
- neskaidra redze
- redzes traucējumi
- deguna asiņošana (deguna asiņošana)
- smagi izsitumi uz ādas (multiformā eritēma, eksfoliatīvs dermatīts)
- patoloģisks neregulārs sirds ritms (priekškambaru mirdzēšana, aritmija, tahikardija), apgrūtināta elpošana (aizdusa).
- ja Jums tiek veikta acu operācija lēcas apduļķošanās (katarakta) vai paaugstināta acs spiediena (glaukoma) dēļ un jūs jau lietojat vai nesen esat lietojis Pradif, zīlīte var slikti paplašināties un varavīksnenes (krāsainā apļveida daļa) acs) operācijas laikā var kļūt ļengans.
- sausa mute.
Ja novērojat jebkādas blakusparādības, kas šajā instrukcijā nav minētas, vai kāda no minētajām blakusparādībām Jums izpaužas smagi, lūdzu, izstāstiet to savam ārstam vai farmaceitam.
Ziņošana par blakusparādībām
Ja Jums rodas jebkādas blakusparādības, konsultējieties ar ārstu vai farmaceitu. Tas attiecas arī uz iespējamām blakusparādībām, kas nav minētas šajā instrukcijā. Jūs varat ziņot par blakusparādībām arī tieši, izmantojot valsts ziņošanas sistēmu vietnē www.agenziafarmaco.gov.it/it/responsabili.Ziņojot par blakusparādībām, jūs varat palīdzēt iegūt vairāk informācijas par šo zāļu drošumu.
Derīguma termiņš un saglabāšana
Uzglabāt oriģinālajā iepakojumā.
Uzglabāt Pradif bērniem nepieejamā un neredzamā vietā.
Nelietot Pradif pēc derīguma termiņa beigām, kas norādīts uz blistera un kastītes pēc “EXP” (mēnesis un gads). Derīguma termiņš attiecas uz mēneša pēdējo dienu.
Zāles nedrīkst izmest kanalizācijā vai sadzīves atkritumos. Jautājiet farmaceitam, kā izmest zāles, kuras vairs nelietojat. Tas palīdzēs aizsargāt vidi.
Sastāvs un zāļu forma
Ko Pradif satur
Aktīvā viela ir tamsulozīna hidrohlorīds.
Citas sastāvdaļas ir: kapsulas saturs: mikrokristāliskā celuloze (E460); metakrilskābes-etilakrilāta kopolimērs (1: 1); polisorbāts 80 (E433); nātrija laurilsulfāts; triacetīns (E1518); kalcija stearāts (E470a); talks (E553b). Kapsulas apvalks: ciets želatīns; indigokarmīns (E132); titāna dioksīds (E171); dzeltenais dzelzs oksīds (E172); sarkanais dzelzs oksīds (E172). Drukas tinte: šellaks (E904), propilēnglikols (E1520), melnais dzelzs oksīds (E172).
Pradif izskata apraksts un iepakojums
Pradif kapsulas ir oranžas / olīvzaļas, marķētas ar T0.4 kodiem un logotipu.
Pradif kapsulas ir iepakotas polipropilēna-alumīnija blisteros, kas atrodas kartona kastē.
Iepakojumā ir 10, 20, 30, 50, 60, 90, 100 vai 200 kapsulas. Visi iepakojuma lielumi tirgū var nebūt pieejami
Avota lietošanas instrukcija: AIFA (Itālijas zāļu aģentūra). Saturs publicēts 2016. gada janvārī. Pašlaik pieejamā informācija var nebūt atjaunināta.
Lai piekļūtu visjaunākajai versijai, ieteicams piekļūt AIFA (Itālijas zāļu aģentūra) vietnei. Atruna un noderīga informācija.
01.0 ZĀĻU NOSAUKUMS
PRADIF CIETAS KAPSULAS
02.0 KVALITATĪVAIS UN KVANTITATĪVAIS SASTĀVS
Katra modificētās darbības kapsula kā aktīvo sastāvdaļu satur 0,4 mg tamsulosīna hidrohlorīda.
Palīgvielas: pilnu palīgvielu sarakstu skatīt apakšpunktā 6.1.
03.0 ZĀĻU FORMA
Oranža / olīvu zaļa modificētas darbības kapsula, cieta, marķēta ar T0.4 kodu un logotipu.
04.0 KLĪNISKĀ INFORMĀCIJA
04.1 Terapeitiskās indikācijas
Apakšējā urīnceļu simptomi (LUTS), kas saistīti ar labdabīgu prostatas hiperplāziju (BPH).
04.2 Devas un lietošanas veids
Iekšķīgai lietošanai.
Viena kapsula dienā, kas jālieto pēc brokastīm vai pēc pirmās ēdienreizes dienā.
Kapsula jānorij vesela, to nedrīkst sasmalcināt vai sakošļāt, jo tas var traucēt aktīvās sastāvdaļas modificēto izdalīšanos.
Nieru darbības traucējumu gadījumā deva nav jāpielāgo.
Vieglas vai vidēji smagas aknu mazspējas gadījumā deva nav jāpielāgo (skatīt arī apakšpunktu 4.3 Kontrindikācijas).
Pediatriskā populācija
Nav norāžu par īpašu Pradif lietošanu bērniem.
Tamsulozīna drošība un efektivitāte bērniem
04.3 Kontrindikācijas
Paaugstināta jutība pret tamsulosīna hidrohlorīdu, ieskaitot zāļu izraisītu angioneirotisko tūsku vai kādu no palīgvielām; ortostatiskas hipotensijas vēsture; smaga aknu mazspēja.
04.4 Īpaši brīdinājumi un piesardzība lietošanā
Tāpat kā citu a1-adrenoreceptoru antagonistu gadījumā, ārstēšanas laikā ar Pradif atsevišķos gadījumos var rasties asinsspiediena pazemināšanās, kas retos gadījumos var izraisīt ģīboni. Pēc pirmajām ortostatiskās hipotensijas pazīmēm (reibonis, vājums) pacientam jāsēž vai jāguļ, līdz simptomi izzūd.
Pirms Pradif terapijas uzsākšanas pacientam jānovērtē, vai nav citu slimību, kas var izraisīt tādus pašus simptomus kā labdabīga prostatas hiperplāzija. Pirms ārstēšanas uzsākšanas un pēc tam ar regulāriem intervāliem jāveic taisnās zarnas izmeklēšana un, ja nepieciešams, prostatas specifiskā antigēna (PSA) noteikšana.
Pacientu ar smagiem nieru darbības traucējumiem (kreatinīna klīrenss ir mazāks par 10 ml / min) ārstēšana jāapsver piesardzīgi, jo zāles nav pētītas šiem pacientiem.
Kataraktas un glaukomas operācijas laikā dažiem pacientiem, kas saņēmuši vai iepriekš ārstējuši tamsulosīna hidrohlorīdu, ir novērots intraoperatīvs flopija varavīksnenes sindroms (IFIS, maza skolēna sindroma variants).
IFIS var palielināt acu komplikāciju risku operācijas laikā un pēc tās.
Tamsulosīna hidrohlorīda lietošanas pārtraukšana 1-2 nedēļas pirms kataraktas vai glaukomas operācijas tiek uzskatīta par empīriski lietderīgu, tomēr ieguvums no ārstēšanas pārtraukšanas vēl nav noskaidrots.
IFIS ir konstatēts arī pacientiem, kuri pirms operācijas bija pārtraukuši tamsulosīna lietošanu ilgāku laiku.
Nav ieteicams uzsākt tamsulosīna hidrohlorīda terapiju pacientiem, kuriem plānota kataraktas vai glaukomas operācija.
Pirmsoperācijas novērtēšanas laikā oftalmologam un ķirurģiskajai komandai jāapsver, vai pacients, kas gaida kataraktas vai glaukomas operāciju, tiek ārstēts vai ir ārstēts ar tamsulosīnu, lai nodrošinātu, ka intervences laikā var veikt atbilstošus pasākumus IFIS pārvaldībai.
Tamsulosīna hidrohlorīdu nedrīkst lietot kombinācijā ar spēcīgiem CYP3A4 inhibitoriem pacientiem ar vāju metabolizējošo CYP2D6 fenotipu.
Tamsulosīna hidrohlorīds jālieto piesardzīgi kombinācijā ar spēcīgiem un mēreniem CYP3A4 inhibitoriem (skatīt 4.5. Apakšpunktu).
04.5 Mijiedarbība ar citām zālēm un citi mijiedarbības veidi
Mijiedarbības pētījumi veikti tikai pieaugušajiem.
Mijiedarbība netika novērota, lietojot tamsulozīna hidrohlorīdu vienlaikus ar atenololu, enalaprilu vai teofilīnu.
Vienlaicīga cimetidīna lietošana izraisa tamsulosīna līmeņa paaugstināšanos plazmā, bet furosemīds to pazemina; tomēr tamsulosīna koncentrācija plazmā ir terapeitiskā diapazonā, tāpēc deva nav jāpielāgo.
In vitro diazepāms, propranolols, trihlormetiazīds, hlormadinons, amitriptilīns, diklofenaks, glibenklamīds, simvastatīns un varfarīns nemaina tamsulosīna brīvo frakciju cilvēka plazmā. Tamsulosīns nemaina diazepāma, propranolola, trihlormetiazīda un hlormadinona brīvo frakciju.
Tomēr diklofenaks un varfarīns var palielināt tamsulosīna eliminācijas ātrumu.
Vienlaicīga tamsulosīna hidrohlorīda un spēcīgu CYP3A4 inhibitoru lietošana var palielināt tamsulosīna hidrohlorīda iedarbību. Vienlaicīga lietošana ar ketokonazolu (zināms spēcīgs CYP3A4 inhibitors) izraisīja tamsulosīna hidrohlorīda AUC un Cmax palielināšanos attiecīgi par 2,8 un 2,2 reizes.
Tamsulosīna hidrohlorīdu nedrīkst lietot kombinācijā ar spēcīgiem CYP3A4 inhibitoriem pacientiem ar vāju metabolizējošo CYP2D6 fenotipu.
Tamsulosīna hidrohlorīds jālieto piesardzīgi kombinācijā ar spēcīgiem un mēreniem CYP3A4 inhibitoriem.
Vienlaicīga tamsulozīna hidrohlorīda un paroksetīna, spēcīga CYP2D6 inhibitora, lietošana izraisīja tamsulosīna Cmax un AUC palielināšanos attiecīgi par 1,3 un 1,6 reizēm, taču šis pieaugums netiek uzskatīts par klīniski nozīmīgu.
Vienlaicīga citu a1 adrenoreceptoru antagonistu lietošana var izraisīt hipotensīvu iedarbību.
04.6 Grūtniecība un zīdīšana
Pradif nav indicēts lietošanai sievietēm.
Īslaicīgos un ilgstošos tamsulosīna hidrohlorīda klīniskajos pētījumos novēroti ejakulācijas traucējumi .. Pēcreģistrācijas pētījumos ir ziņots par ejakulācijas traucējumu gadījumiem, retrogrādu ejakulāciju un nespēju ejakulēt.
04.7 Ietekme uz spēju vadīt transportlīdzekļus un apkalpot mehānismus
Nav veikti pētījumi par spēju vadīt transportlīdzekļus un apkalpot mehānismus, tomēr pacientam jāapzinās reiboņa iespējamība.
04.8 Nevēlamās blakusparādības
* Novērots pēcreģistrācijas periodā
Kataraktas un glaukomas operācijas laikā pēcreģistrācijas uzraudzības periodā ir novērots mazs skolēna sindroma variants, kas pazīstams kā "Intraoperatīvs flopija varavīksnenes sindroms" (IFIS), kas saistīts ar tamsulosīna terapiju (skatīt arī apakšpunktu 4.4).
Pēcreģistrācijas pieredze: papildus iepriekš uzskaitītajām blakusparādībām saistībā ar tamsulozīna lietošanu ir ziņots par priekškambaru mirdzēšanu, aritmiju, tahikardiju un aizdusu. Tā kā šie spontāni ziņotie notikumi ir iegūti pēcreģistrācijas pieredzē visā pasaulē, biežumu un tamsulosīna lomu to izraisīšanā nevar droši noteikt.
Ziņošana par iespējamām blakusparādībām
Ir svarīgi ziņot par iespējamām blakusparādībām, kas radušās pēc zāļu reģistrācijas, jo tas ļauj nepārtraukti uzraudzīt zāļu ieguvuma un riska attiecību. Veselības aprūpes speciālistus lūdz ziņot par visām iespējamām blakusparādībām, izmantojot valsts ziņošanas sistēmu. "Adrese www. agenziafarmaco.gov.it/it/responsabili.
04.9 Pārdozēšana
Simptomi
Pārdozēšana ar tamsulosīna hidrohlorīdu var izraisīt smagu hipotensīvu iedarbību.
Dažādos pārdozēšanas līmeņos tika novērota smaga hipotensīva iedarbība.
Ārstēšana
Akūtas hipotensijas gadījumā pēc pārdozēšanas nekavējoties jārīkojas, lai atbalstītu sirds un asinsvadu sistēmu.
Asinsspiedienu un sirdsdarbības ātrumu var atjaunot, liekot pacientam apgulties.
Ja ar to nepietiek, var izmantot tilpuma paplašinātājus un, ja nepieciešams, vazokonstriktīvas zāles. Ir jāuzrauga nieru darbība un jāpiemēro vispārēji atbalstoši pasākumi.
Dialīze ir maz noderīga, jo tamsulozīns spēcīgi saistās ar plazmas olbaltumvielām. Lai novērstu absorbciju, var veikt dažus pasākumus, piemēram, vemšanu.
Ja norītas lielas devas, var būt noderīga kuņģa skalošana, un var ievadīt aktivēto ogli un osmotisko caureju, piemēram, nātrija sulfātu.
05.0 FARMAKOLOĢISKĀS ĪPAŠĪBAS
05.1 Farmakodinamiskās īpašības
Farmakoterapeitiskā grupa: a1 adrenoreceptoru antagonists.
ATĶ kods: G04C A02.
Preparāti ekskluzīvai prostatas patoloģiju ārstēšanai.
Darbības mehānisms:
tamsulosīns selektīvi un konkurētspējīgi saistās ar postsinaptiskiem a1 adrenoreceptoriem, jo īpaši a1A un a1D apakštipiem. Tas izraisa prostatas un urīnizvadkanāla gludo muskuļu atslābināšanos.
Farmakodinamiskā iedarbība:
pradif palielina maksimālo urīna plūsmu. Novērš šķēršļus, atslābinot prostatas un urīnizvadkanāla gludos muskuļus, tādējādi uzlabojot urinēšanas simptomus.
Tas arī uzlabo uzpildes simptomus, kuros urīnpūšļa nestabilitātei ir svarīga loma.
Šī ietekme uz uzpildīšanas un iztukšošanas simptomiem saglabājas ilgstošas terapijas laikā. Operācijas vai kateterizācijas nepieciešamība ir ievērojami aizkavējusies.
A1 adrenoreceptoru antagonisti var samazināt asinsspiedienu, samazinot perifēro pretestību. Klīniskajos pētījumos ar Pradif netika novērota klīniski nozīmīga asinsspiediena pazemināšanās.
Pediatriskā populācija
Bērniem ar neiropātisku urīnpūsli tika veikts dubultmaskēts, randomizēts, placebo kontrolēts, devu diapazona pētījums. Kopumā 161 bērns (2-16 gadus veci) tika randomizēts un ārstēts ar 1 no 3 tamsulosīna devas līmeņiem (zems [0,001 līdz 0,002 mg / kg], vidējs [0,002 līdz 0,004 mg / kg] un augsts [0,004 līdz 0,008 mg / kg]) vai ar placebo. Primārais parametrs bija to pacientu skaits, kuru izzušanas punkta detrusora spiediens (detrusora noplūdes punkta spiediens, LPP) samazinājās līdz hidronefrozes un hidrouretera stabilizācijai un urīna tilpuma izmaiņām, kas iegūtas kateterizācijas rezultātā, un urīna noplūdes skaitam kateterizācijas laikā, kā ierakstīts katetrizācijas dienasgrāmatās. Nebija būtiskas atšķirības starp placebo grupu un kādu no 3 tamsulosīna grupām ne primārajiem, ne sekundārajiem mērķa kritērijiem.
05.2 Farmakokinētiskās īpašības
Uzsūkšanās
Tamsulozīna hidrohlorīds uzsūcas no zarnām un ir gandrīz pilnībā bioloģiski pieejams.
Lietojot to tuvu ēdienreizēm, tamsulosīna hidrohlorīda uzsūkšanās samazinās.
Vienotu uzsūkšanos var panākt, ja pacients vienmēr lieto Pradif pēc vienas un tās pašas ēdienreizes.
Tamsulosīnam piemīt lineāra kinētika.
Pēc vienas Pradif devas ēdienreizē tamsulosīna līmenis plazmā sasniedz maksimumu aptuveni 6 stundu laikā, un līdzsvara stāvokļa apstākļos, kas tiek sasniegts pēc 5 ārstēšanas dienām, Cmax ir aptuveni par 2/3 augstāks nekā pēc vienas devas.
Tas ir atzīmēts gados vecākiem pacientiem, un ir pamatoti gaidīt to pašu jaunākiem pacientiem.
Pēc vienreizējas un atkārtotas devas lietošanas plazmas līmenis ievērojami atšķiras.
Izplatīšana
Cilvēkiem tamsulosīns saistās ar plazmas olbaltumvielām aptuveni 99%, izkliedes tilpums ir zems (aptuveni 0,2 l / kg).
Biotransformācija
Tamsulosīnam ir vāja pirmās caurlaides iedarbība, jo tas tiek lēni metabolizēts.
Tamsulosīns plazmā atrodas galvenokārt nemainītas aktīvās sastāvdaļas veidā.
Tas tiek metabolizēts aknās.
Žurkām praktiski netika novērota tamsulosīna izraisīta mikrosomu aknu enzīmu sistēmas indukcija.
In vitro rezultāti liecina, ka CYP3A4 un arī CYP2D6 ir iesaistīti metabolismā, iespējams, neliels ieguldījums tamsulosīna hidrohlorīda metabolismā, ko veic citi CYP izoenzīmi. Zāles metabolizējošo enzīmu CYP3A4 un CYP2D6 inhibīcija var palielināt tamsulosīna hidrohlorīda iedarbību (skatīt 4.4. Un 4.5. Apakšpunktu).
Neviens no metabolītiem nav aktīvāks par sākotnējo produktu.
Eliminācija
Tamsulosīns un tā metabolīti galvenokārt izdalās ar urīnu un aptuveni 9% devas nemainītas aktīvās vielas veidā.
Pēc vienas Pradif devas barošanas un līdzsvara stāvokļa apstākļos eliminācijas pusperiods tika novērtēts attiecīgi pēc 10 un 13 stundām.
05.3 Preklīniskie drošības dati
Vienreizējas un atkārtotas devas toksicitātes pētījumi tika veikti ar pelēm, žurkām un suņiem. Tika apsvērti arī reprodukcijas pētījumi ar žurkām, kancerogenitātes pētījumi ar pelēm un žurkām, genotoksicitātes pētījumi. in vivo un in vitro.
Vispārējais toksikoloģiskais profils, kas noskaidrots, lietojot lielākas tamsulozīna devas, atbilst zināmajai a1 adrenoreceptoru antagonistu zāļu farmakoloģiskajai aktivitātei.
Suņiem, lietojot ļoti lielas devas, elektrokardiogramma tiek mainīta.Šī reakcija nav klīniski nozīmīga.
Tamsulosīnam nav būtisku genotoksisku īpašību.
"Ir ziņots par palielinātu proliferatīvo izmaiņu biežumu žurku un peļu mātītē. Šie atklājumi, kurus, visticamāk, izraisa hiperprolaktinēmija un rodas tikai lielās devās, tiek uzskatīti par nebūtiskiem."
06.0 FARMACEITISKĀ INFORMĀCIJA
06.1 Palīgvielas
Kapsulas saturs:
mikrokristāliskā celuloze E460, metakrilskābe - etilakrilāta kopolimērs (1: 1), polisorbāts 80 E433, nātrija laurilsulfāts, triacetīns E1518, kalcija stearāts E470a, talks E553b.
Kapsula:
cietais želatīns, indigokarmīns E132, titāna dioksīds E171, dzeltenais dzelzs oksīds E172, sarkanais dzelzs oksīds E172.
Drukas tinte:
šellaks E904, propilēnglikols E1520, melnais dzelzs oksīds E172.
06.2 Nesaderība
Nav būtisks.
06.3 Derīguma termiņš
4 gadi.
06.4 Īpaši uzglabāšanas nosacījumi
Uzglabāt oriģinālajā iepakojumā.
06.5 Tiešā iepakojuma veids un iepakojuma saturs
Polipropilēns - alumīnija blisteri pa 10 kapsulām, kastītēs pa 10, 20, 30, 50, 60, 90, 100 un 200 kapsulām.
PVC / PVDC - alumīnija blisteris ar 5 kapsulām, iepakojumā pa 50 kapsulām.
Visi iepakojuma lielumi tirgū var nebūt pieejami.
06.6 Norādījumi lietošanai un lietošanai
Nav īpašu norādījumu.
07.0 REĢISTRĀCIJAS APLIECĪBAS ĪPAŠNIEKS
Boehringer Ingelheim International GmbH - Binger Strasse 173 - D 55216 Ingelheim am Rhein - Vācija
Itālijas pārstāvis
Boehringer Ingelheim Italia S.p.A. - Via Lorenzini, 8 - 20139 Milāna
08.0 REĢISTRĀCIJAS APLIECĪBAS NUMURS
Kastīte ar 20 kapsulām: A.I.C. Nr. 030106013
Iepakojumā 30 kapsulas: A.I.C. N ° 030106025
09.0 PIRMĀJAS APLIECĪBAS VAI ATĻAUJAS DATUMS
1996. gada 27. septembris/2006. gada 12. jūlijs.
10.0 TEKSTA PĀRSKATĪŠANAS DATUMS
10.06.2014.










.jpg)