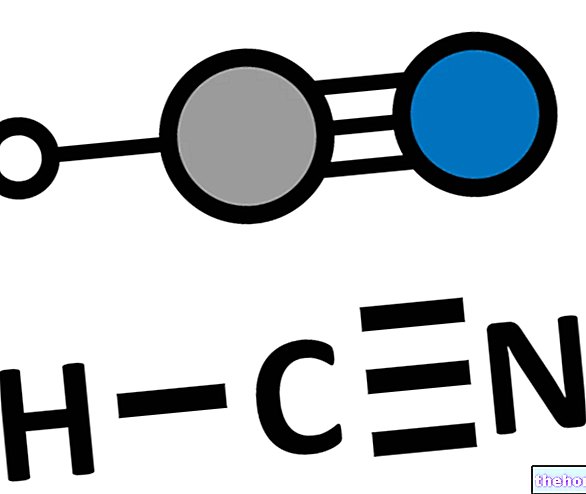
Kad bioaktivizēts, tetrahlorogleklis (CCl4, sarežģīta molekula un pats par sevi nav ļoti toksisks) noved pie notikumu ķēdes un daudzu toksisku savienojumu veidošanās. Šī molekula ir pazīstama arī ar nosaukumu FREON 10.
Freon 10 agrāk tika izmantots kā ugunsdzēšamo aparātu, ledusskapju, gaisa kondicionētāju, traipu tīrīšanas līdzekļu un ķīmiskās tīrīšanas šķidruma sastāvdaļa.
Freons 10 ir ļoti bīstams, jo tas zaudē elektronu, kad tas tiek metabolizēts trihlormetilēnā (CCl3); šim pēdējam metabolītam ir nesapārots elektrons, tāpēc tas kļūst par radikālu, tāpēc ļoti reaģējošu savienojumu. Trihlormetilēnam ir daudz bīstamu efektu:
- tas viegli saistās ar -EME olbaltumvielu grupu;
- bloķē citohroma P450 aktivitāti (jo citohroms ir "hemoproteīns");
- iedarbojas uz citiem šūnu proteīniem;
- var izraisīt aknu nekrozi un vēzi;
- tas var izraisīt nefropātijas;
- mijiedarbojoties ar membrānas lipīdu taukskābēm, tas noved pie hloroforma veidošanās, kas oksidējoties noved pie fosgēna veidošanās.
Agrāk hloroformu izmantoja kā anestēzijas līdzekli; tā patiesībā ir ļoti toksiska viela, jo tā rezultātā veidojas ļoti toksisks oglekļa tetrahlorīda metabolīts.

Arī no Freon 10 mēs iegūstam PHOSGENE, kas ir ļoti toksisks metabolīts. Jo īpaši no visiem metabolītiem, kas veidojas, metabolizējoties freonam 10, fosgēns, salīdzinot ar citiem, nepārprotami ir toksiskākais.
Mūsu ķermeņa fosgēna metabolīts tiek kavēts ar "hidrolīzes darbību, kas to sadala sālsskābē (HCl) un oglekļa dioksīdā (CO2). Tomēr, ja šī inhibīcijas sistēma ir nepietiekama, fosgēns neatgriezeniski saistās ar kovalentajām saitēm." Ar visiem proteīniem.
Citi raksti par tēmu "Oglekļa tetrahlorīds vai freons 10"
- Dibrometāns: ietekme uz veselību
- Toksicitāte un toksikoloģija
- Aromātiskie amīni un ēdienu gatavošana